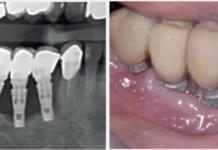
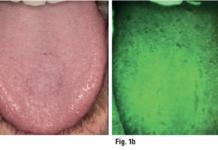
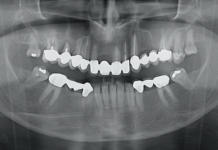
L’odontoiatra è un operatore sanitario che molto spesso si confronta con il sintomo dolore, sia acuto (pulpite, parodontite acuta eccetera) che cronico (parodontite cronica, dolori muscolari, disturbi dell’ATM eccetera).
A volte il dolore è il solo sintomo che conduce il paziente più riluttante nello studio odontoiatrico ed il successo dipende dall’alleviamento del dolore stesso.
L’introduzione degli anestetici locali nella pratica clinica ha completamente cambiato l’approccio alle cure odontoiatriche: l’anestesia locale e il conseguente controllo effettivo del dolore da procedure odontoiatriche formano oggi le basi per la pratica odontoiatrica moderna. Grazie all’anestesia locale, oggi si effettuano grandi interventi chirurgici a carico dei mascellari (ottavi inclusi, implantologia, rialzo del seno eccetera) senza che il paziente accusi alcun tipo di dolore durante gli interventi stessi.
Per la maggior parte delle persone la paura del trattamento odontoiatrico si centra attorno all’elemento dolore e spesso tale sintomo è associato alla figura del dentista; le persone che si devono sottoporre alle cure odontoiatriche sono soggetti solitamente prevenuti e timorosi verso il sintomo dolore e per una parte di questi il fattore che più causa paura è la puntura dell’ago nel cavo orale (1).
La letteratura si è sempre interessata della ricerca di nuove procedure che consentano di ridurre il disagio provocato dalla puntura dell’ago (1).
Infatti il dolore che a tutt’oggi è ancora poco controllato è quello dovuto all’iniezione locale dell’anestetico; tale dolore possiamo definirlo inutile, non necessario perché non svolge funzione di sentinella o di campanello d’allarme per una patologia: l’Associazione Internazionale per lo Studio del Dolore (IASP) definisce, infatti, il dolore come un “evento spiacevole associato ad un danno attuale o potenziale dei tessuti” (2, 3).
Ecco perché è importante cercare soprattutto di diminuire o annullare la sensazione dolorosa della puntura dell’ago e della contestuale iniezione del farmaco che, una volta in loco, inizierà il suo effetto anestetico.
Scopo del lavoro è stato quello di valutare l’incidenza del dolore durante l’anestesia locale, cercando di capire come il paziente si pone verso questo sintomo e stabilire la soglia di tolleranza dello stesso al sintomo dolore, durante l’iniezione dell’anestetico, mettendo in atto, se necessario, procedure che possano ridurre tale percezione.
È pur vero che fattori psicologici, quali precedenti esperienze con il dolore, fiducia nella procedura o nell’abilità del dentista o del medico, personalità generale, back-ground culturale, ansia, suggestionabilità e così via, giocano un ruolo in tutti i metodi di controllo del dolore.
Inoltre in alcuni pazienti, che definiamo come soggetti fobici, si manifestano dei fenomeni, di destrutturazione e di regressione (dal punto di vista psicoanalitico) che lo riportano indietro nel tempo alla sua condizione di bambino, indifeso e insicuro; tale fenomeno regressivo nel paziente si manifesta attraverso il corpo, in particolare nell’incontro tra quello che è un gelido strumento (siringa odontoiatrica con relativo ago) e la sua bocca: un organo primitivo di fondamentale importanza, attraverso il quale passano tutte le espressioni, i sentimenti, le emozioni, il piacere (4, 5).
Per quanto detto sopra, è molto importante misurare e quantificare a tutti i pazienti, l’intensità del dolore avvertito durante l’iniezione dell’anestetico tramite semplici scale (VAS e NRS): il fine è quello di meglio comprendere sia la soglia di tolleranza al dolore, come detto sopra, da parte del paziente che abbiamo di fronte, sia la possibilità di mettere in atto successivamente, verso il paziente stesso, procedure per ridurre l’intensità dello stimolo doloroso.
La legge 38 del 2010 ha inoltre istituzionalizzato, per l’operatore sanitario, la rilevazione del dolore all’interno della cartella clinica al fine di assicurare il rispetto della dignità della persona umana.
Infatti ogni paziente ha un corpo e una psiche: l’approccio, come metodica di fondo, deve essere pertanto olistico. Cercare di capire, da parte dell’operatore sanitario, con chi si ha a che fare sotto il profilo umano-esistenziale è una esigenza sempre più sentita in vari settori professionali: il paziente è sempre degno di una attenta ed obiettiva conoscenza allo scopo di poter instaurare con lui una relazione adeguata e comprendere se reagisce in modo razionale o irrazionale.
Cercare di capire l’Io di una persona è anche sapere come questo si pone verso il sintomo dolore: “dolore è ciò che è descritto dalla persona che lo prova, ogni qual volta lo affermi” (6), pur sapendo che la poltrona odontoiatrica ha una potenzialità destrutturante l’insieme delle percezioni dell’Io stesso (4).
In definitiva il dentista, sia attraverso una buona e doverosa anamnesi, sia attraverso una capacità introspettiva ed empatica, deve riuscire a “inquadrare” chi ha di fronte per trattarlo in modo adeguato e, quanto più possibile, in modo indolore.
Siccome l’alleviamento del dolore deve essere l’obiettivo di ogni fase di pratica sanitaria, la comprensione dello stesso richiede conoscenze di neuroanatomia, fisiologia, psicologia e farmacologia da parte del clinico (7).
Dal punto di vista anatomo-fisiologico, il sistema algico (pain system), a grandi linee, può essere suddiviso in tre parti (8):
- sistema di conduzione (afferenziale) che trasmette gli impulsi nocicettivi dalla periferia al centro;
- sistema di riconoscimento e risposta a livello corticale;
- sistema di modulazione e controllo che, a livello midollare e a livello del nucleo caudale-spinale del trigemino, riduce la potenza degli stimoli dolorosi afferenti (cancello);
a questa suddivisione semplice e schematica in tre sistemi bisogna aggiungere, per meglio definire il sistema algico, le cellule della glia che dialogano con i neuroni sia a livello centrale che midollare attraverso il cosiddetto sistema delle chinasi (9).
Le fibre nervose, collegate ai nocicettori periferici, che trasportano lo stimolo dolorifico al midollo spinale sono di due tipi: fibre A mieliniche (alta velocità di conduzione) e fibre C amieliniche ( bassa velocità di conduzione); le fibre A sono suddivise in A alfa, A beta, A gamma e A delta: proprio quest’ultime, responsabili del dolore acuto, sono le fibre implicate nel trasporto degli stimoli dolorosi di tipo meccanico e termico ad alta intensità ed hanno una soglia di eccitabilità più bassa rispetto alle fibre C ; quest’ultime, a loro volta responsabili del dolore cronico, sono collegate a recettori polimodali che rispondono oltre che a stimoli termici e meccanici anche a stimoli elettrici e chimici (8, 10).
Le fibre A alfa, beta e gamma sono responsabili della sensibilità tattile e propriocettiva ed hanno una velocità di conduzione molto maggiore sia delle fibre A delta che delle C (11).
MATERIALI E METODI
Rilevazione VAS-NRS
L’anestesia nel cavo orale si suddivide in plessica, ligamentosa e tronculare: la plessica e la ligamentosa vengono praticate mediante aghi molto sottili (30G 0,3x16); come anestetico è stata usata la mepivicaina al 2% con adrenalina 1/100000: il dolore percepito dal paziente è dovuto alla puntura dell’ago vera e propria e poi alla iniezione del liquido anestetico che penetra nei tessuti della sottomucosa scollandoli.
Tutte le procedure anestesiologiche messe in atto in questo lavoro sono state praticate dallo stesso odontoiatra.
A tutti i pazienti che hanno necessitato di procedure anestesiologiche, da alcuni anni e dopo la stessa, è stata mostrata la scala di VAS (scala analogica visiva) che riporta sul retro una scala di valutazione numerica (scala NRS da 0 a 10) (12) (figg. 1 e 2).
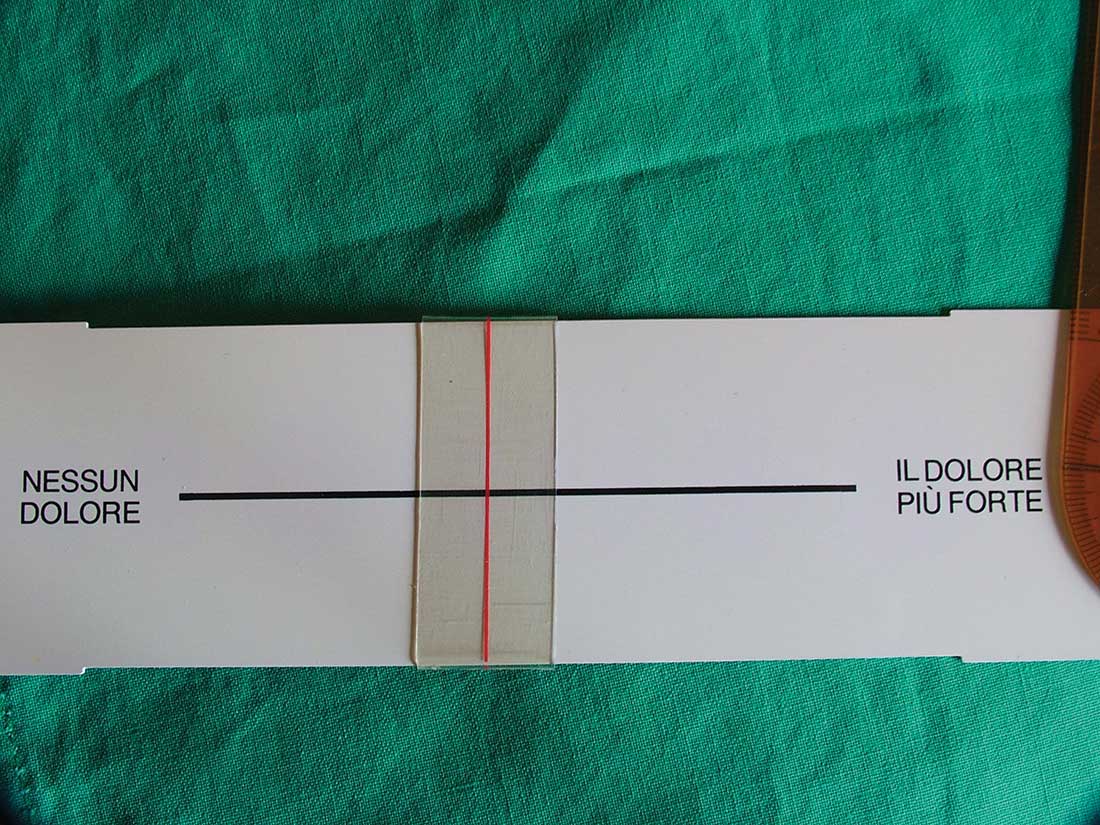

Ai pazienti è stato chiesto di indicare sulla scala di VAS, tramite cursore, l’intensità del dolore avvertito sia per la puntura dell’ago che per la successiva iniezione. In questo modo la valutazione visiva del paziente è stata tradotta subito in valutazione numerica e quindi archiviata come media della doppia rilevazione.
La scala numerica (NRS) viene normalmente suddivisa in quattro parti:
- 0 nessun dolore (classe 0);
- da 1 a 3 che corrisponde al dolore lieve (classe I);
- da 4 a 7 che corrisponde al dolore moderato (classe II);
- da 8 a 10 che corrisponde al dolore grave o severo (classe III).
Lo studio è stato di tipo osservazionale retrospettivo su 276 pazienti (147 femmine e 129 maschi) a cui è stato richiesto regolare consenso informato che è stato realizzato in accordo con gli standard etici stabiliti nella Dichiarazione di Helsinki del 1964.
Ai pazienti è stata praticata anestesia locale, per cure odontoiatriche o estrazioni, sia di tipo plessico-ligamentosa, sul versante vestibolare o palato-linguale, che tronculare; tutti i pazienti reclutati sono stati divisi in 3 gruppi:
- pazienti fino a 18 anni;
- pazienti da 19 a 65 anni;
- pazienti ultrasessantacinquenni.
Tutti i pazienti dei 3 gruppi suddetti, in base alla intensità del dolore avvertito e segnalato dopo la procedura anestesiologica, sono stati suddivisi ed inseriti nelle quattro classi della scala NRS.
Presso-vibrazione periprocedura anestesiologica (PVPA)
Allo scopo di ridurre il dolore da anestesia, sulla mucosa orale si applica, attualmente, lo spray a base di lidocaina al 10% e al 15% o le creme sempre a base di lidocaina al 5% o di lidocaina+benzocaina (uso off label). In questo lavoro si è cercato di dare un contributo alla soluzione di tale problematica valutando, su alcuni pazienti, l’applicazione nella zona dove viene praticata l’iniezione di una stimolazione presso-vibratoria; è stato utilizzato uno strumento ultrasonico nato per tutt’altra indicazione (Vibringe) (fig. 3).
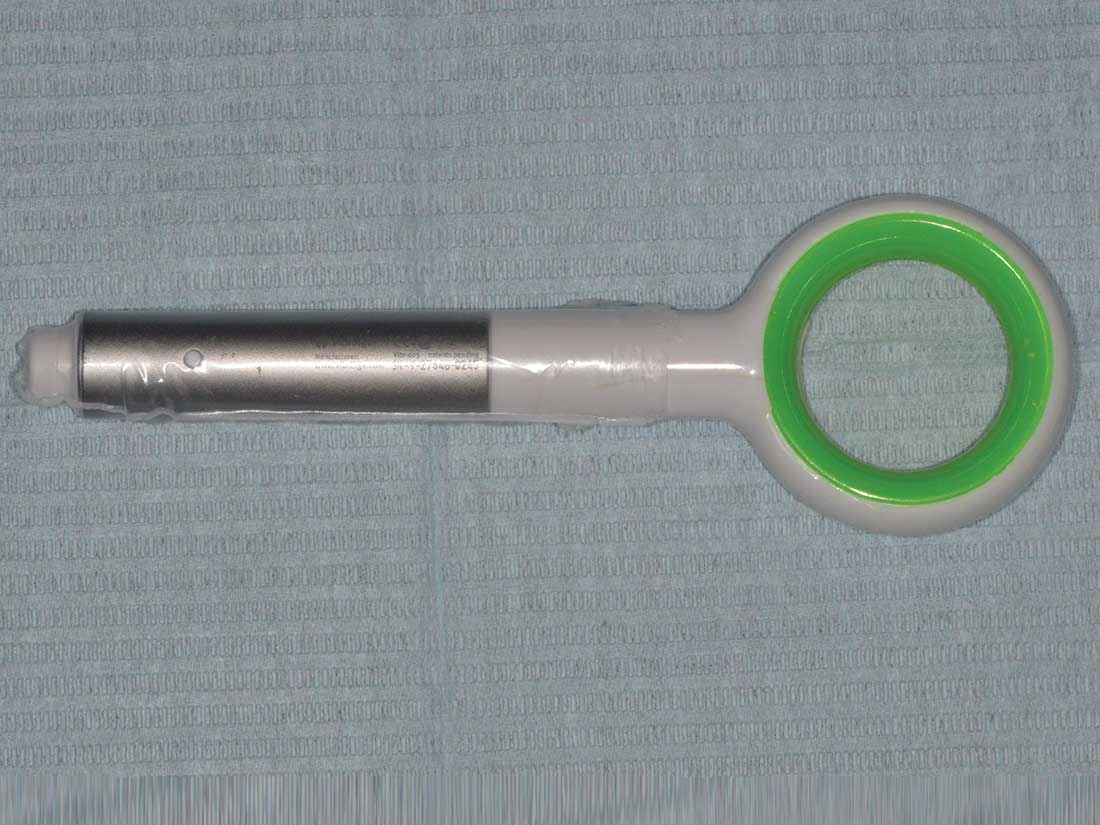
Sin dall’inizio degli anni ‘80, gli studi sul dolore sono stati indirizzati alla ricerca di soluzioni alternative al problema del dolore dell’ago; in particolare è stato studiato l’effetto dello stimolo vibratorio durante le procedure anestetiche, come dimostrano gli studi di Lundeberg e Ottason (10, 11, 13, 14). Negli anni successivi si è assistito a un susseguirsi di lavori che hanno utilizzato la vibrazione come metodologia per alleviare il dolore (15, 16, 17) come dimostrano i lavori di Kakjgi (18) e Hutchins (19).
In pratica si può usare qualsiasi presidio che provochi tale tipo di stimolazione presso-vibratoria: la definiamo, pertanto, presso-vibrazione periprocedura anestesiologica (PVPA) (fig. 4).
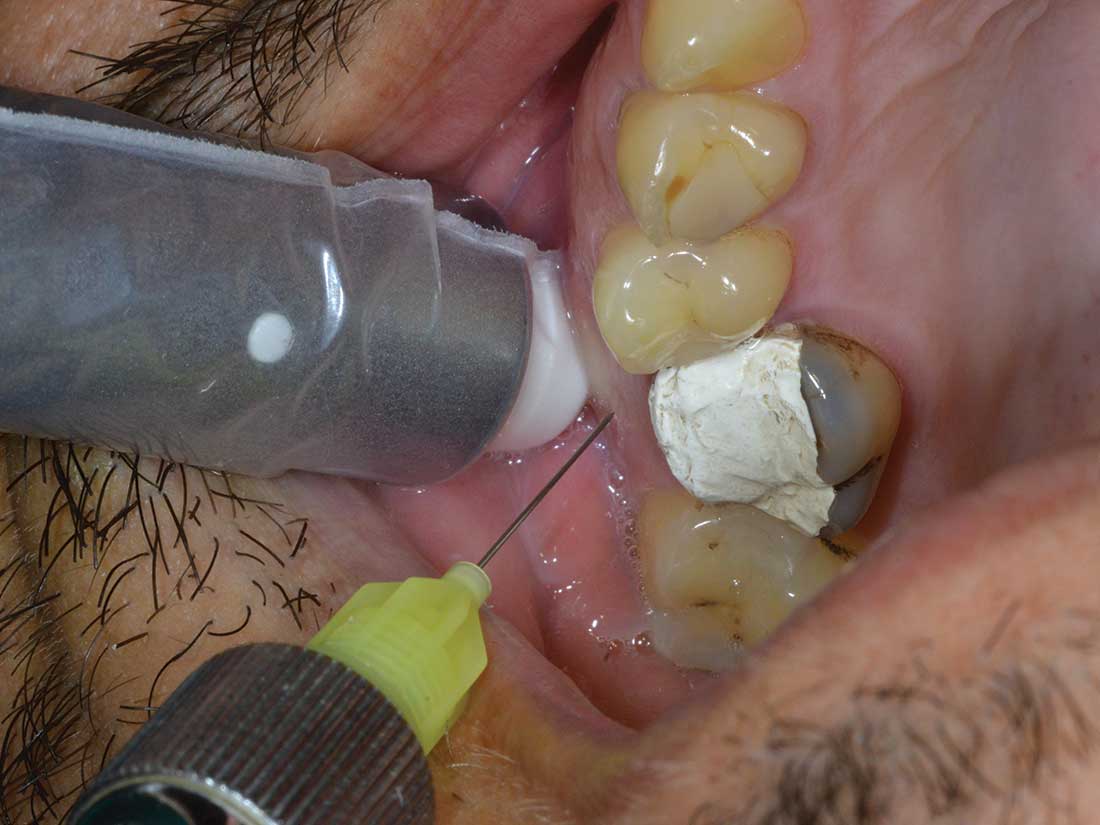
La procedura operativa da noi utilizzata ha previsto le seguenti fasi:
- divaricazione dei tessuti molli con l’ausilio della parte terminale dello strumento che si poggia in vicinanza del punto dove andrà fatta l’anestesia;
- attivazione della presso-vibrazione;
- esecuzione della puntura con l’iniezione dell’anestetico;
- rimozione dell’ago e dello strumento vibratorio.
Al paziente è stata quindi mostrata la scala VAS-NRS per indicare l’intensità del dolore avvertito.
Il principio è vecchio: risale infatti al 1965 quando Melzack e Wall (20, 21) teorizzarono il fenomeno del cancello a livello midollare; oggi il fenomeno è meglio spiegato con i neuroni modulatori presenti nella sostanza gelatinosa del midollo.
Da quanto detto, a proposito della velocità di conduzione di uno stimolo, e partendo dal presupposto, già noto ai fisiologi dell’800, che la trasmissione del dolore è in ritardo rispetto alla trasmissione sensoriale (6), uno stimolo tattile-propriocettivo (pressione+vibrazione) di intensità tale da non provocare dolore, arrivando prima al midollo spinale, che come sappiamo rappresenta uno dei cardini della modulazione nocicettiva, determina una attivazione di meccanismi modulatori localizzati a livello della sostanza gelatinosa (SG): trattasi di interneuroni agenti tramite inibizione presinaptica per mezzo di neurotrasmettitori tipo encefalina, GABA, glicina ed altri (22).
Lo scopo è di ridurre l’intensità dei potenziali d’azione (PA) afferenti al cervello perché tali PA, determinando una continua e massiccia depolarizzazione della membrana dei neuroni corticali, possono provocarne la sofferenza (22).
Una volta attivato lo stimolo tattile-propriocettivo, eventuali stimoli dolorifici che arrivano a livello midollare o, come nel nostro caso, al nucleo caudato del trigemino, dal I neurone troveranno un II neurone, che come sappiamo trasmette sia gli stimoli dolorifici che tattili-proprocettivi(neuroni WDR o polimodali), con una modesta capacità di trasmettere lo stimolo dolorifico verso il talamo: troveranno cioè il cosiddetto cancello chiuso. Certamente la cosiddetta modulazione spinale non si spiega soltanto attraverso il meccanismo del suddetto “gate controll” teorizzato da Melzack e Wall nel 1965, ma è molto più complessa e articolata (23), tuttavia ciò non è argomento di questo lavoro.
Gli anestetici locali, una volta iniettati nel tessuto, prevengono la formazione e la conduzione dell’impulso nervoso: si legano a specifici recettori all’interno del poro dei canali per il NA+ presenti sulla membrana eccitabile dei nervi e impediscono il movimento ionico attraverso di esso e il susseguente generarsi di un potenziale d’azione ad alta frequenza che è alla base della percezione dolorifica.
La PVPA è stata applicata in casi di anestesia plessica o ligamentosa su pazienti già precedentemente trattati e inseriti nella I, II o III classe NRS; la procedura non può essere applicata in caso di anestesia tronculare, soprattutto del nervo mandibolare.
RISULTATI
25 pazienti (12 femmine e 13 maschi) nel gruppo fino a 18 anni di cui 4 in classe 0 (16%), 12 in classe I (48%); 8 in classe II (32%); 1 in classe III (4%).
La presso-vibrazione è stata applicata e valutata su 8 pazienti:
- 2 di classe I, dove è risultata efficace portando i pazienti in classe 0;
- 5 di classe II: in 2 pazienti la procedura è risultata efficace facendo scendere i pazienti di una classe e in 3 non efficace;
- 1 paziente di classe III in cui è risultata efficace portando il paziente in II classe.
La presso-vibrazione è risultata, quindi, efficace in 5 pazienti (62,5%).
192 pazienti (104 femmine e 88 maschi) nel gruppo tra 19 e 64 anni di cui 48 pazienti in classe 0 (25%), 79 pazienti in classe I (41,1%), 57 pazienti in classe II (29,6%), 8 pazienti in classe III (4,1%).
La presso-vibrazione è stata applicata e valutata su 49 pazienti:
- 14 di classe I: in 11 pazienti è risultata efficace portando gli stessi in classe 0, in 3 non è risultata efficace;
- 28 di classe II: in 22 è risultata efficace portando i pazienti stessi in I classe e in 6 pazienti non è risultata efficace;
- 7 di classe III: in 3 è risultata efficace e in 4 no.
La procedura presso-vibratoria è risultata efficace in 36 pazienti (73,4%).
59 pazienti ultrasessantacinquenni (31 femmine e 28 maschi) di cui 7 in classe 0 (11,8%), 28 in classe I (47,4%), 18 in classe II (30,5%), 6 in classe III (10,1%).
La presso-vibrazione è stata valutata su 15 pazienti con questi risultati:
- 5 pazienti di classe I: in 4 non è risultata efficace e in 1 paziente è risultata efficace;
- 7 pazienti di classe II: in 5 è risultata efficace e in 2 no;
- 3 pazienti di classe III: in 2 è risulata inefficace e in 1 paziente è risultata efficace.
La procedura è risultata efficace in 7 pazienti (46,6%).
La PVPA è stata, quindi, applicata e valutata in totale su 71 pazienti. È risultata efficace su 47 pazienti (66,2%).
80 pazienti dei 276 inclusi nello studio sono stati trattati con anestesia tronculare all’alveolare inferiore tramite siringa monouso da 2,5 cc con ago standard 22 G (0,7x32mm), dove, come detto sopra, non è stata applicata la procedura di presso-vibrazione ed è stata utilizzato come anestetico la mepivicaina al 3% senza vasocostrittore, il dolore rilevato è stato il seguente:
pazienti fino a 18 anni, 14 iniezioni con media di 2,9 della scala NRS (dolore lieve);
pazienti tra 19 e 64 anni, 50 iniezioni con media 2,8 della scala NRS (dolore lieve);
pazienti ultrasessantacinquenni, 16 iniezioni con media 3,3 della scala NRS (dolore moderato).
DISCUSSIONE
Non vi è significativa differenza di genere tra i pazienti inseriti nelle 4 classi della scala NRS, né vi è differenza di genere significativa tra i pazienti su cui si è dimostrata efficace o meno la PVPA.
I valori della scala numerica sono tendenzialmente più alti per le procedure anestesiologiche dal lato linguale e palatale: ciò si spiega perché la mucosa e sottomucosa del cavo orale, su tali versanti, è molto aderente al periostio e quindi è necessaria una pressione maggiore per la penetrazione dell’ago e dell’anestetico.
Peraltro, bisogna anche dire che la testina piatta dello strumento a vibrazione ultrasonico, che come abbiamo suddetto è nato per altri scopi, mal si adatta alle superfici concave del palato e del versante linguale della mandibola e che uno strumento allo scopo dedicato potrebbe certamente ridurre i valori della scala del dolore anche su tali zone del cavo orale; quantificare la percezione del dolore da parte dei pazienti può aiutare altri ricercatori a sviluppare apparecchi che funzionano ancor meglio di quelli sperimentati negli ultimi anni da Nasehi, Saijo, Shahidi Bonjar e Nanitson (24, 25, 26, 27).
Valori numerici più alti sulla scala del dolore si riscontrano anche nei pazienti al di sopra dei 65 anni (vedi la percentuale più bassa di pazienti in classe 0, la percentuale più alta di pazienti in classe III e la media piu alta, sulla scala NRS, nei pazienti trattati con anestesia tronculare), che con più probabilità hanno sofferto, durante la loro vita, di dolore cronico a carico del cavo orale dovuto in particolar modo a malattia parodontale.
Ciò è spiegabile con il concetto della neuroplasticità e cioè la sensibilizzazione periferica e centrale delle fibre nervose indotta, in corso di dolore cronico, dalle neurotrofine e soprattutto dal Nerve Growth Factor (NGF). L’infiammazione cronica favorisce la liberazione di NGF da parte soprattutto dei mastociti; l’NGF, a livello delle terminazioni nervose, si lega al recettore TRK-A (tirosinchinasi A) che invierà un messaggio al ganglio spinale corrispondente (per il trigemino il ganglio di Gasser) di tipo trascrizionale per produrre sia nuovi recettori a livello periferico, che abbassano la soglia del dolore, sia sostanze sensibilizzanti a livello midollare (sostanza P) che ne aumentano l’eccitabilità (9).
La minore efficacia della presso-vibrazione peri-procedura anestesiologica nei pazienti >di 65 anni (46,6%) può essere spiegata, ugualmente, con la sensibilizzazione della via nocicettiva dovuta a pregressi stati di infiammazione cronica dei tessuti duri e molli del cavo orale; in alcuni pazienti era la stessa vibrazione ad essere avvertita come fonte di dolore (iperalgesia e allodinia).
L’infiammazione cronica provoca, a livello periferico, anche il risveglio di recettori particolari chiamati tetratossina resistenti (TTXr): la tetratossina è un potente anestetico locale e la presenza di recettori TTXr potrebbe essere una ulteriore causa per spiegare l’inefficacia degli anestetici locali quando vengono iniettati in zone con infiammazione in atto (9).
CONCLUSIONI
È molto utile approcciare tutti i pazienti che necessitano di cure odontoiatriche quantificando il dolore avvertito durante l’iniezione dell’anestetico, in modo tale da sapere e scrivere in cartella se gli stessi necessitano di procedure per ridurlo; il sintomo dolore e la sua quantificazione, nello spirito della legge 38, deve essere il sesto parametro vitale, oltre alla pressione arteriosa, alla frequenza cardiaca, alla frequenza respiratoria, alla saturazione di O2 (tramite pulsossimetro), alla temperatura corporea, da prendere sempre in considerazione quando si approccia qualsiasi tipo di paziente. Quantificare il dolore tramite le scale VAS-NRS è anche un modo migliore per comunicare e dialogare con i colleghi e la comunità scientifica.
Per quel che riguarda la PVPA, che può essere messa in atto contestualmente all’anestesia plessica o ligamentosa nel cavo orale, possiamo affermare che la stessa riduce, con buona percentuale (66,2%), il dolore dovuto alla puntura ed all’iniezione dell’anestetico.
Ridurre la percezione del dolore procurato dalla puntura dell’ago aumenta l’aderenza dei pazienti alle cure odontoiatriche e si riduce anche il numero di persone che hanno paura delle procedure odontoiatriche stesse; e siccome, come asserisce M. de Montaigne (filosofo francese, 1533-1592) aver paura di sentire dolore è già soffrire, ridurre il numero di persone che hanno paura significa ridurre la sofferenza e, certamente, questa procedura aiuta a raggiungere tale scopo, che dovrebbe essere uno dei fini di tutti gli operatori sanitari. ●
- Davoudi A, Rismanchian M, Akhavan A, Nosouhian S, Bajoghli F, Haghighat A et al. A brief review on the efficacy of different possible and nonpharmacological techniques in eliminating discomfort of local anesthesia injection during dental procedures. Anesth Essays Res 2016 Jan-Apr; 10(1):13-6.
- IASP Task Force on Taxonomy: Part III: Pain Terms, a Current List with Definitions and Notes on Usage. In Classification of Chronic Pain. 2 edition. Edited by Merskey H, Bogduk N. WA, Seattle; IASP Press; 1994:209-14.
- Rodella Luigi F. Intervista. Teamwork Clinic 2016; 18(4):16.
- Melica VM. Come trattare con l’odontopaziente. Recordati Documenti Scientifici; 1989.
- Cancellada F. La regressione del paziente odontoiatrico. Tesi di ricerca presso la facoltà di Scienze della formazione Carlo Bò di Urbino; 2010.
- McCaffery M, Beebe A. Pain: Clinical Manual for Nursing Practice. St Louis: CV Mosby Company; 1989.
- La Clinica Odontoiatrica del Nord America. Il Dolore. Padova: Piccin Editore 1982;11(3).
- Tiengo M. Le vie del dolore e la loro patologia. Brexin Library; 1991.
- Sabato AF. Dolore basi molecolari. CIC Edizioni Internazionali 2010.
- Ottoson D, Ekblom A, Hasson P. Vibratory stimulation for the relief of pain of dental origin. Pain 1981; 10:37-45.
- Lundeberg T, Abrahamsson P, Bondesson L, Haker E. Effect of vibratory stimulation on experimental and clinical pain. Scand J Rehabil Med 1988;20:149-69.
- Di Sabatino V, Biasi G. Dolore prevenire la cronicizzazione. Algosflogos 2012; supplemento al n. 2 di Medico e Paziente.
- Lundeberg T, Nordemar R, Ottoson D. Pain alleviation by vibration stimulation. Pain 1984;20:25-44.
- Lundeberg T, Ottoson D, Hakansson S, Meyerson BA. Vibratory stimulation for the control of intractable chronic orofacial pain. Advances in Pain Research and Therapy 1983;5:555–61.
- www.popsci.it. Finalmente: una tecnologia che rende le iniezioni indolori. ASA Press Release online 2014, pubblicato il 13/10.
- Milani AS, Zand V, Abdollahi AA, Froughreyan M, Zakeri-Milani P, Iafarabadi MA. Effect of topical anesthesia with lidocaine-prilocaine(EMLA) cream and local pressure on pain during infiltration injection for maxillary canines: a randomized double-blind clinical trial. J Contemp Dent Pract 2016 Jul;17(7):592-6.
- Shilpapriva M, Javanthi M, Reddy VN, Sakthivel R, Selvaraiu G, Viavakumar P. Effectveness of new vibration delivery system on pain associated with injection of local anesthesia in children. J Indian Soc Pedod Prev Dent 2015 Jul-Sep;33(3):173-6. Doi: 10.4103/0970-4388.160343
- Kakigi R, Shibasaki H. Mechanisms of pain relief by vibration and movement. J Neurol Neurosurg Psychiatry 1992;55:282-6.
- Hutchins HS Jr, Young FA, Lackland DT, Fishburne CP. The effectiveness of topical anesthesia and vibration in alleviating the pain of oral injections. Anesth Prog 1997;44:87–9.
- Melzach R, Wall PD. Pain mechanism: a new theory. Science 1965 Nov;150(3699):971-9.
- Sufka KJ, Price DD. Gate Control Theory reconsidered. Brain Mind 2002;2:277-90.
- Molina M, Magnano G. Il dolore oro-cranio-facciale.Milano: Ilic’ Editrice; 2005.
- Nori SL, Manfrida S, Barbi S, Valentini V. Guida pratica al riconoscimento delle vie anatomiche del dolore. Roma: Eco Edizioni Internazionali; 2008.
- Nasehi A, Bardwaj S, Kamath AT, Gaticherla S, Pentapati KC. Shahidi. Clinical pain evaluation with intraoral vibration device during local anesthetic injection. J Clin Exp Dent 2015 Feb 1;7(1):e23-7. Doi: 10.4217jced.51643. eCollection 2015
- Saijo M, Ito E, Ichinohe T, Kaneko Y. Lack of pain reduction by a vibrating local anesthetic attachment: a pilot study. Anesth Prog. 2005 Summer;52(2):62-4.
- Shahidi Bonjar AH. Syringe micro vibrator ( SMV) a new device being introduced in dentistry to allievate pain and anxiety of intraoral injection, and a comparative study with a similar device. Ann Surg Innov Res 2011 Jan;7,5(1):1. Doi:10.1186/1750-1164-5.
- Nanitson E, R Vartuli, A Forte, PJ Dennison, CC Peck. The effectof vibration on pain during local anesthesia injection. Australian Dental Journal 2010;54-94. Doi:10.1111/j.1834-7819.2009