REAZIONI AVVERSE A FARMACO A LIVELLO DELLA CAVITÀ ORALE
Il cavo orale costituisce un complesso sistema di strutture, ciascuna delle quali ospita una variegata comunità microbica e svolge un ruolo cruciale nelle molteplici funzioni dell’apparato stomatognatico, quali digestione, respirazione, fonazione e gusto (1). Rivestita da mucosa orale, distinta in cheratinizzata e non cheratinizzata, questa superficie presenta peculiarità anatomiche: la mucosa cheratinizzata, situata nelle zone maggiormente esposte a stress meccanici. Oltre alle variazioni nella cheratinizzazione, si osservano differenze specifiche del sito in termini di spessore mucosale e turnover cellulare (2). La mucosa orale svolge diverse funzioni vitali, quali quella di barriera fisica contro stimoli meccanici e chimici, la lubrificazione del cavo orale attraverso la secrezione salivare delle ghiandole salivari minori, e partecipa alla percezione sensoriale di stimoli termici, tattili e algici. Tuttavia, a causa delle sue peculiari caratteristiche, la mucosa orale rappresenta un bersaglio frequente di tossicità derivante da alcuni tipi di terapie farmacologiche, sia locali che sistemiche.
Le reazioni avverse a farmaci in campo odontostomatologico, ossia a carico della cavità orale (adverse drug reactions in oral cavity, ADR-O), si manifestano in modi diversi e non sono indicative di una singola associazione con uno specifico principio attivo. L’introduzione continua di nuovi farmaci sul mercato, insieme a nuove indicazioni cliniche e la possibilità di interazioni tra farmaci, richiede una sorveglianza attenta ADR-O.
Tutte le reazioni avverse ai farmaci (adverse drug reactions, ADR), comprese le ADR-O, possono essere suddivise in base al loro meccanismo d’azione e alla loro natura (3).
Per quanto riguarda la classificazione basata sul meccanismo d’azione, le ADR possono essere distinte come segue: ▼

La classificazione in base alla natura delle ADR, inizialmente proposta da Rawlins e Thompson, include 6 diversi tipi: di tipo A (aumentate), B (imprevedibili), C (croniche), D (ritardate), E (alla sospensione) e F (fallimento) (5), come riportato in tabella 1.

Le ADR-O comprendono principalmente lesioni quali erosioni o ulcere, difetti dell’epitelio che possono derivare da diverse cause, tra cui l’azione diretta del farmaco, reazioni immunitarie. Nel panorama delle reazioni avverse ai farmaci che coinvolgono la cavità orale emergono specifici agenti farmacologici destinati a malattie sistemiche anche molto comuni. Tra questi agenti, gli anticonvulsivanti, i calcio-antagonisti e gli immunomodulatori spesso sono correlati a un aumento del tessuto gengivale (6) come ACE-inibitori, gli anestetici locali e diversi tipi di antibiotici possono innescare edema della mucosa orale, coinvolgendo diverse parti come labbra, lingua e occasionalmente l’ugola (edema di Quincke); queste stesse classi di farmaci possono essere anche associate all’insorgenza di cheilite (7). L’assunzione di antibiotici, corticosteroidi o immunomodulatori può causare infezioni opportunistiche da Candida spp. nella cavità orale. Le reazioni avverse ai farmaci orali (ADR-O) possono inoltre manifestarsi come eritema multiforme, una condizione caratterizzata da lesioni rosse, talvolta con vescicole, che possono coinvolgere l’intera mucosa orale. Tale reazione può essere scatenata da antibiotici, anticonvulsivanti, antiretrovirali e farmaci antinfiammatori non steroidei (FANS) (8). Inoltre, alcuni individui possono sviluppare un’eruzione cutanea fissa da farmaco, una condizione in cui l’aspetto e la posizione della eruzione sono consistenti a ogni esposizione al farmaco. Questo fenomeno, spesso associato ad anestetici, antibiotici, antisettici, collutori, nonché utilizzo di dentifrici, rappresenta un ulteriore aspetto delle reazioni avverse ai farmaci che coinvolgono la cavità orale (9).
Di seguito verranno analizzate le più importanti manifestazioni di ADR-O con coinvolgimento della mucosa orale, passando da quelle più rare che possono avere manifestazioni tanto severe da mettere a rischio la vita a quelle meno severe ma più frequenti. Inoltre, sarà analizzata la comparsa di lesioni orali conseguenti alla vaccinazione anti-SARS-CoV-2, concentrandosi sulle reazioni avverse osservate in questo contesto specifico. Verranno attenzionate, infine, particolari categorie di pazienti a rischio ADR-O, ovvero coloro che stanno affrontando trattamenti farmacologici antitumorali e che sono soggetti allo sviluppo di lesioni orali che si configurano anche sotto forma di lesioni ulcerative che possono influenzare significativamente la loro qualità di vita.
ERITEMA MULTIFORME E SINDROMI CORRELATE
L’eritema multiforme (EM) e le sindromi associate rappresentano un insieme di condizioni acute che possono avere un interessamento multifocale, sia cutaneo che mucoso (10). In passato, si riteneva che l’herpes simplex virus (HSV) fosse la causa principale di queste manifestazioni, tuttavia, ricerche recenti hanno evidenziato numerosi casi di EM causati da farmaci (11). È interessante notare che queste manifestazioni possono anche limitarsi esclusivamente alla cavità orale.
Esistono tre forme principali di EM, classificate in ordine crescente di gravità:
- la sindrome di Lyell, conosciuta anche come necrolisi epidermica tossica (TEN), è considerata la forma più grave;
- la sindrome di Steven-Johnson (SJS), o EM maggiore;
- EM minore.
La TEN e la SJS sono reazioni infiammatorie severe che coinvolgono i linfociti T citotossici e si manifestano attraverso lesioni vescicolo-bollose che coinvolgono la pelle e le mucose, con un esteso distacco epidermico e necrosi. Le manifestazioni cliniche di questi disturbi variano notevolmente in termini di severità e possono coinvolgere la pelle e le mucose, con oltre il 90% dei pazienti che presenta coinvolgimento mucoso, tra cui la mucosa orale, oculare o genitale. Sintomi simil-influenzali come febbre, affaticamento e linfoadenopatie possono precedere le eruzioni cutanee.
La TEN si caratterizza per chiazze eritematose, lesioni cutanee con aspetto a bersaglio, estese erosioni mucose e bolle con distacco epidermico che possono interessare oltre il 30% della superficie corporea. La SJS coinvolge la cute in modo simmetrico e almeno due mucose diverse, con un coinvolgimento della superficie corporea inferiore al 10%.
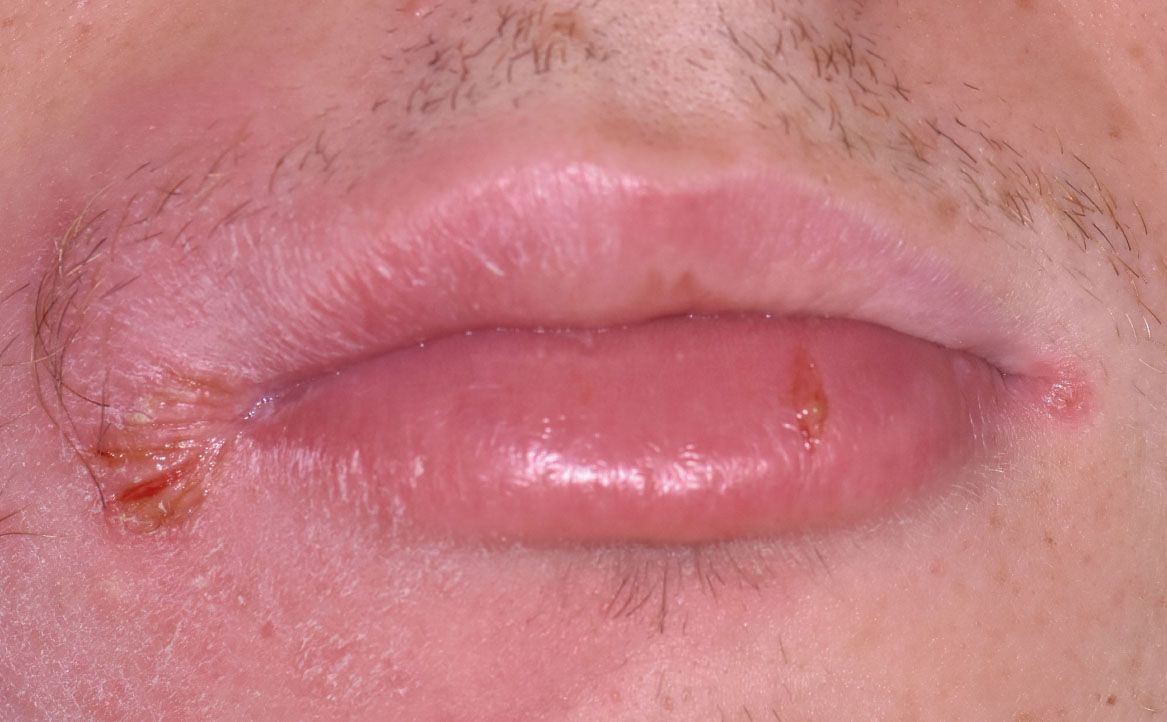
L’EM minore si manifesta con lesioni simmetriche che coprono meno del 10% della superficie corporea (fig. 1). Clinicamente, nelle lesioni della cavità orale si osservano eritema, vescicole e ulcere, con particolare coinvolgimento del labbro, che può sviluppare croste emorragiche (12).
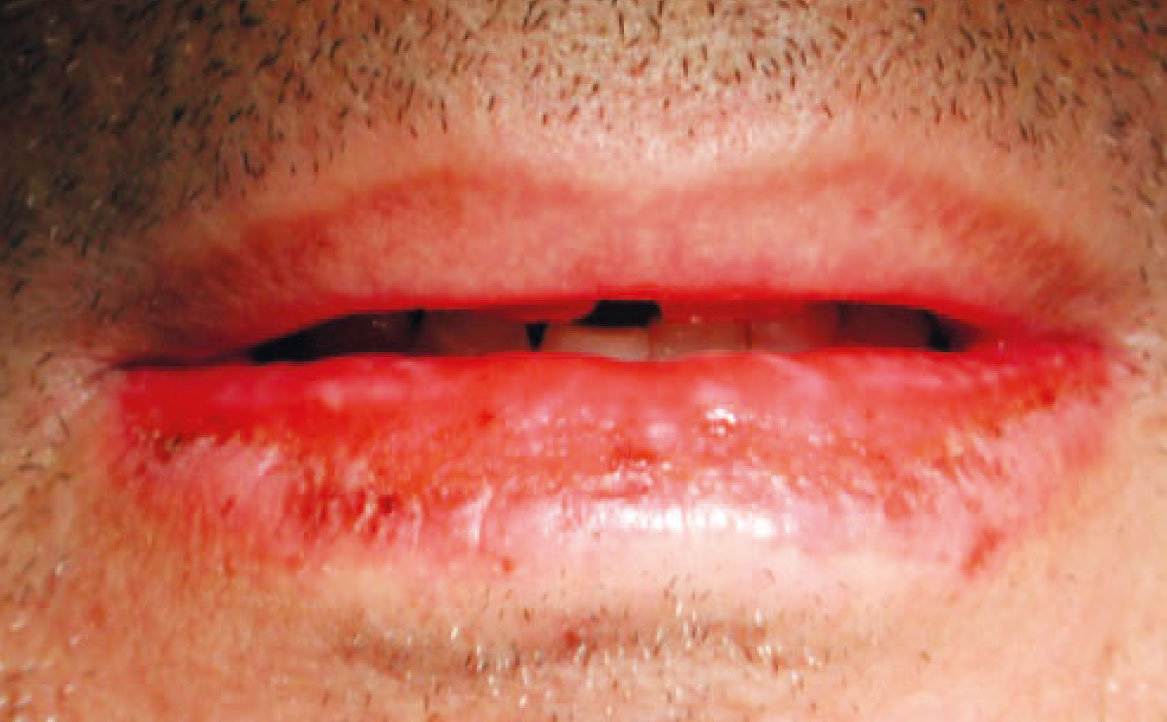
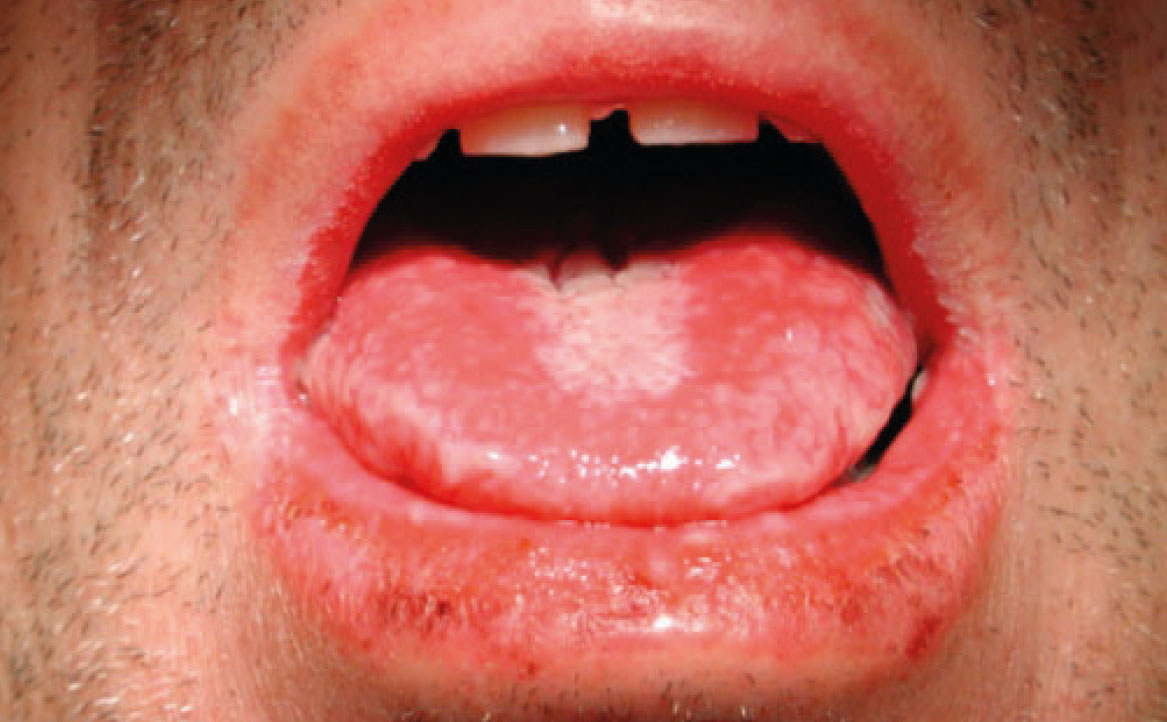
La diagnosi di EM farmaco-indotta si basa sulla presentazione clinica e sulla storia clinica del paziente. Tra il 18% e il 25% dei casi di EM è associato all’uso di farmaci come i FANS e alcuni antibiotici (penicillina, cefalosporina, tetraciclina, clindamicina e rifampicina), ma l’elenco dei farmaci coinvolti continua ad aumentare, compresi quelli biologici.
Non sembra esserci una predilezione di genere per queste condizioni, e possono manifestarsi in pazienti di tutte le età, dall’infanzia all’età avanzata. Tuttavia, l’età media dei pazienti con SJS è di circa 25 anni, mentre per la TEN è di circa 63 anni. La mucosa orale è spesso coinvolta, con una frequenza che varia dal 25% al 70% (13).
ANGIOEDEMA
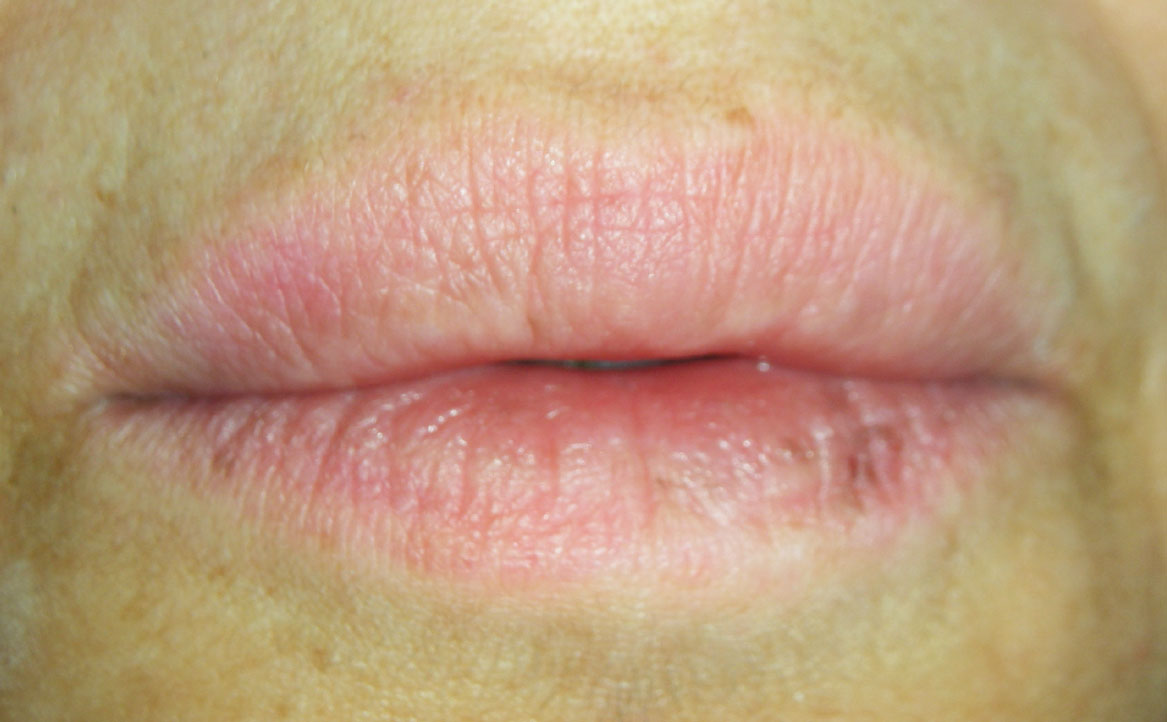
L’angioedema è caratterizzato da un edema causato dall’incremento della permeabilità dell’endotelio vascolare in una specifica regione del corpo, che porta alla fuoriuscita di liquido plasmatico dai capillari nei tessuti più profondi del derma, del sottocute e della sottomucosa. Nei casi in cui coinvolge la cavità orale, in particolare le labbra e la lingua, e le vie aeree superiori, si manifesta con sintomi come dispnea, respiro sibilante e difficoltà nella fonazione, con possibili conseguenze gravi dovute all’ostruzione delle vie respiratorie (14). La diagnosi dell’angioedema indotto da farmaci si basa sulla valutazione clinica e sull’anamnesi del paziente. Gli ACE-inibitori e i FANS sono i farmaci più frequentemente associati a questa condizione (15). Per quanto riguarda gli ACE-inibitori, l’angioedema è causato dall’inibizione dell’enzima responsabile della degradazione della bradichinina nei tessuti, che porta all’aumento della permeabilità vascolare. Questo evento avverso può verificarsi rapidamente o anche molti anni dopo l’inizio del trattamento con ACE-inibitori. Per quanto riguarda i FANS, essi provocano una reazione di ipersensibilità mediata dalle IgE, che porta alla degranulazione dei mastociti e alla liberazione di mediatori chimici, come l’istamina, con conseguente vasodilatazione e aumento della permeabilità vascolare (fig. 2). L’incidenza di angioedema associato agli ACE-inibitori è di circa il 2%, mentre per i FANS è dello 0,1-0,3% nei pazienti che li assumono. Altre classi di farmaci, come i bloccanti dei recettori dell’angiotensina, la simvastatina, l’aspirina e altri, sono stati segnalati come potenziali induttori di angioedema (16).
REAZIONI LICHENOIDI
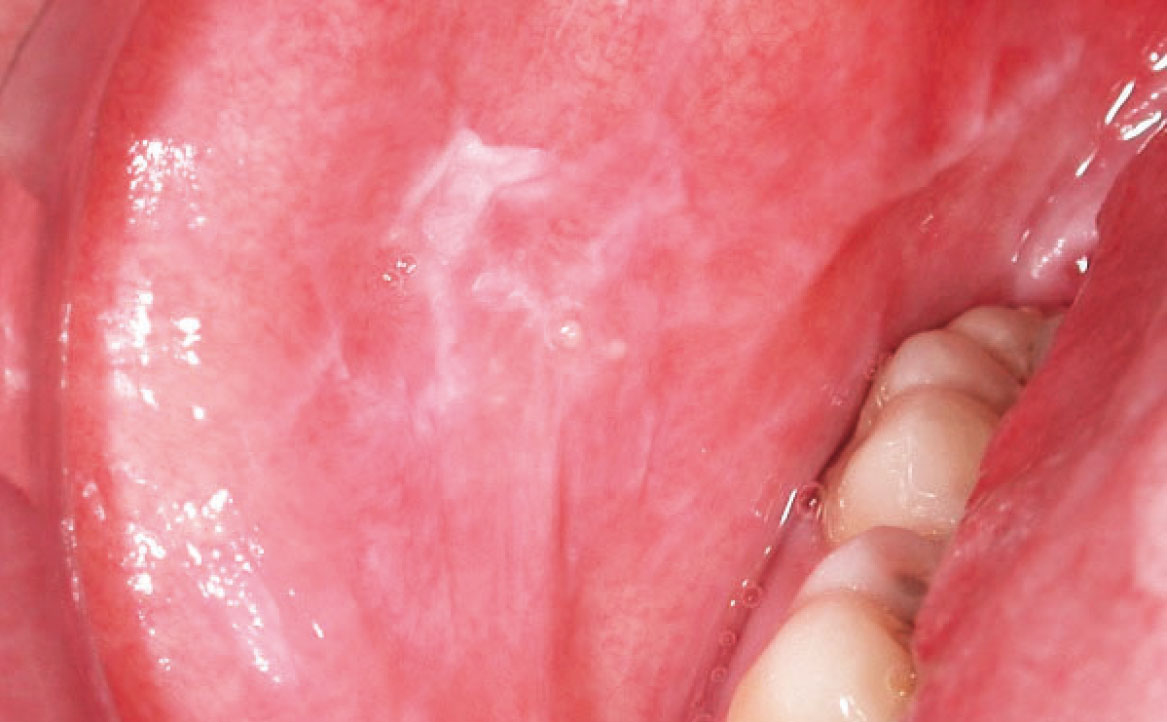
Le reazioni o lesioni lichenoidi orali presentano una similitudine clinica con le lesioni da lichen planus orale, sebbene si distinguano per una marcata componente eritematosa/erosiva e una distribuzione unilaterale delle lesioni, in particolare sulla mucosa geniena e sul dorso e margine laterale della lingua. Inoltre, a differenza del lichen planus, queste reazioni consentono di individuare la causa scatenante e vengono classificate in base all’agente causale coinvolto, che può essere il contatto diretto con materiali di restauro dentale o lesioni farmaco-correlate (17).
I più recenti criteri diagnostici utilizzati per queste lesioni sono stati proposti nel 2020 dal WHO Collaborating Centre for Oral Cancer in the UK (18), i cui criteri comprendono le entità delle lesioni lichenoidi orali (oral lichenoid lesions, OLL) per identificare quei casi in cui i criteri clinici e/o istologici per lichen planus non erano completamente soddisfatti, annoverando tra le OLL più entità cliniche, tra cui le reazioni lichenoidi da contatto (cibi e sostanze) e da farmaco.
Le manifestazioni cliniche di OLL rientrano nei quadri di mucosite cellulo-mediata dell’interfaccia (interface cell-mediated mucositis, ICMM), caratterizzata dalla presenza di un significativo infiltrato infiammatorio cronico a ridosso dell’interfaccia epitelio-stromale associata a una risposta immunitaria cellulo-mediata basata sull’azione citotossica dei linfociti T e rivolta contro i cheratinociti dello strato basale. Il riscontro di questo fenotipo istologico nella diagnostica delle patologie della mucosa orale è relativamente frequente, ma la sua interpretazione non è univoca. La possibile insorgenza di una ICMM a seguito dell’assunzione di un farmaco deve essere considerata reazione avversa al farmaco a patogenesi immunologica. Lo sviluppo di OLL da farmaco si basa sulla capacità di farmaci attivi di attivare specifici antigeni sui cheratinociti, portando all’insorgenza della condizione. I farmaci, agendo come apteni, si legano alle proteine cellulari, diventando così immunogeni. Questi allergeni vengono catturati dalle cellule di Langherans, che li trasportano ai linfonodi dove stimolano una risposta immunitaria. Alcuni farmaci possono anche alterare proteine di superficie, innescando una reazione allergica. Sebbene talvolta la reazione possa risolversi senza la rimozione del farmaco, in altri casi persiste anche dopo la sua sospensione. A livello istologico, queste lesioni sono caratterizzate da un infiltrato infiammatorio con presenza di plasmacellule ed eosinofili nella lamina propria, tuttavia, queste caratteristiche non sono sempre presenti, rendendo difficile distinguere le forme da farmaco dalle forme idiopatiche di lesioni lichenoidi, ma contraddistinguendo una condizione di ICMM.
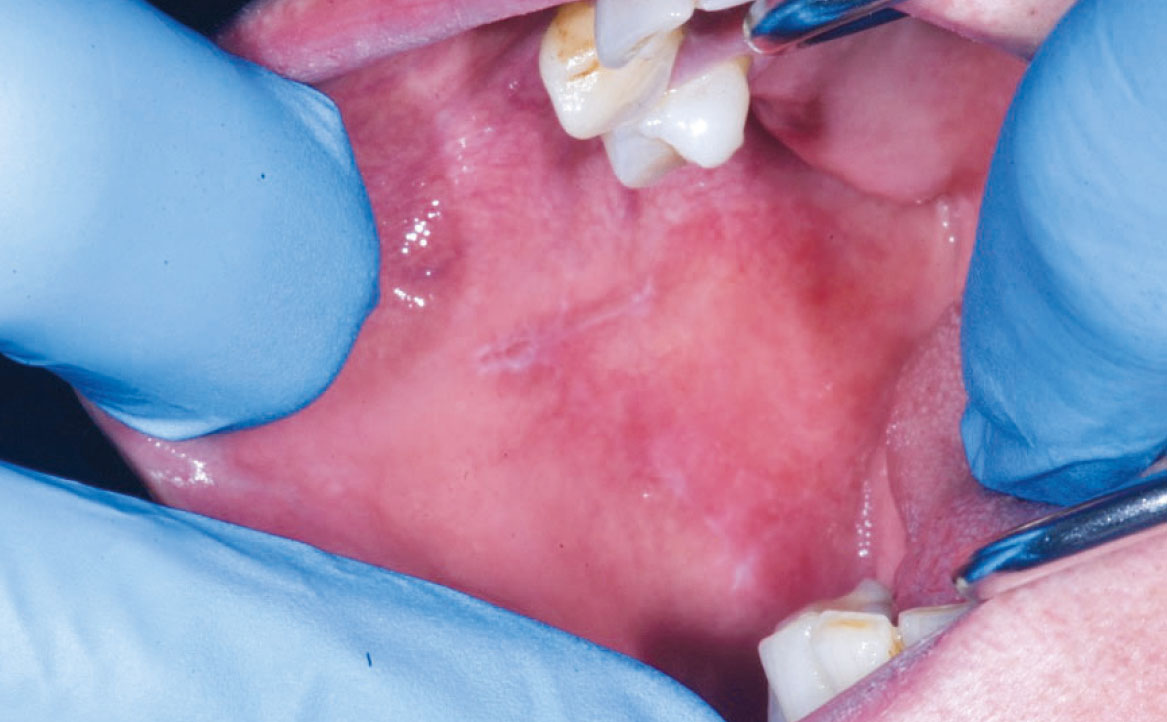
Più di 50 diversi farmaci sono stati associati a questo tipo di lesioni, tra cui i più comuni sono gli antipertensivi, compresi i β-bloccanti, gli ACE inibitori e i diuretici. In aggiunta, anche farmaci antidiabetici come le sulfaniluree (tolbutamide e glipizide), antimicotici come il ketoconazolo, anticonvulsivanti come la carbamazepina, farmaci immunomodulatori come i sali d’oro e la penicillamina, la sulfasalazina e l’allopurinolo sono stati segnalati come agenti responsabili delle LR (fig. 3) Questi farmaci sono spesso utilizzati in combinazione, suggerendo un possibile effetto sinergico (19).
LUPUS ERITEMATOSO
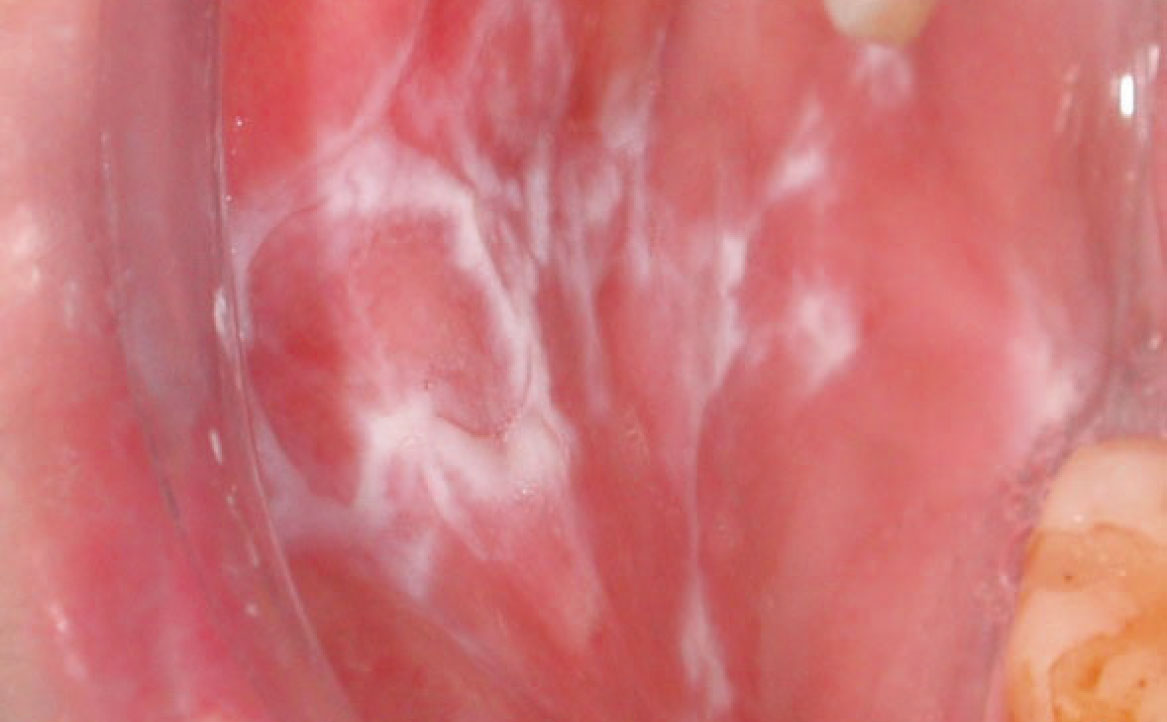
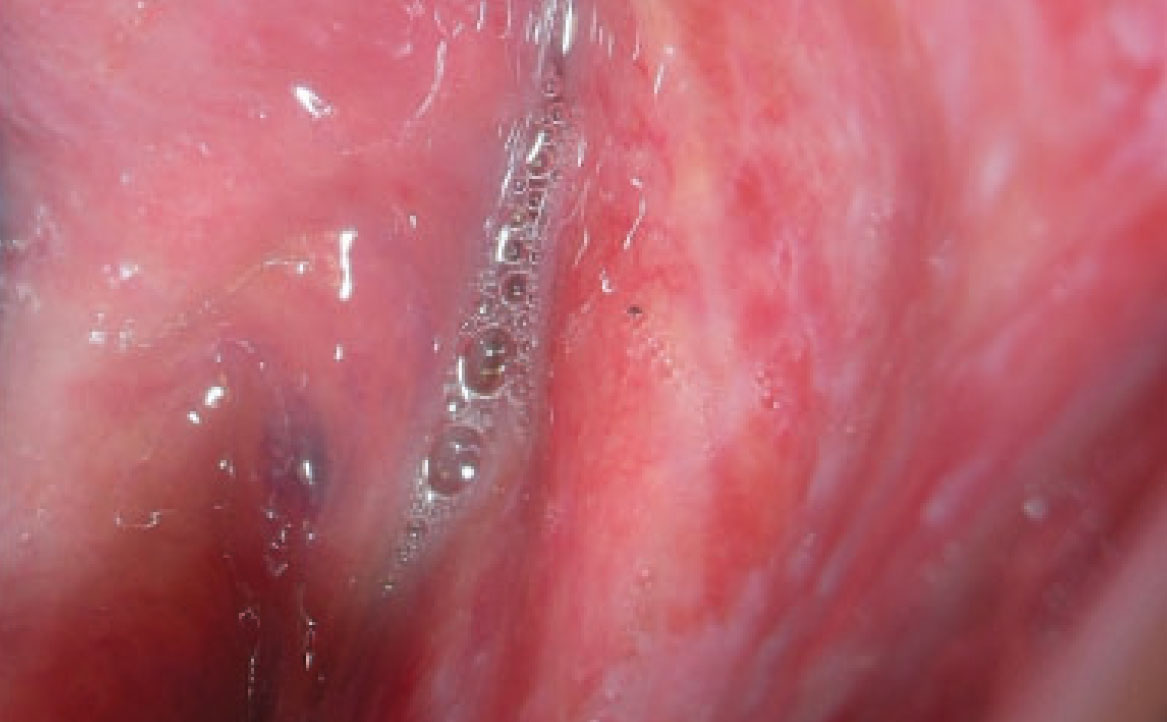
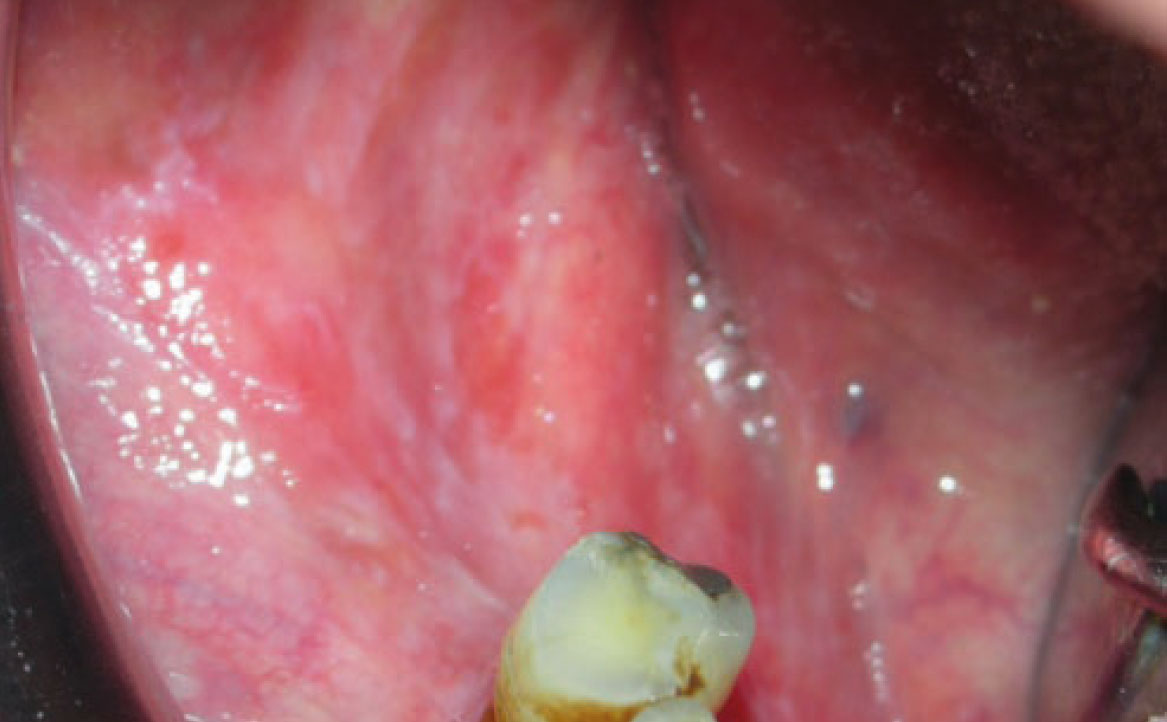
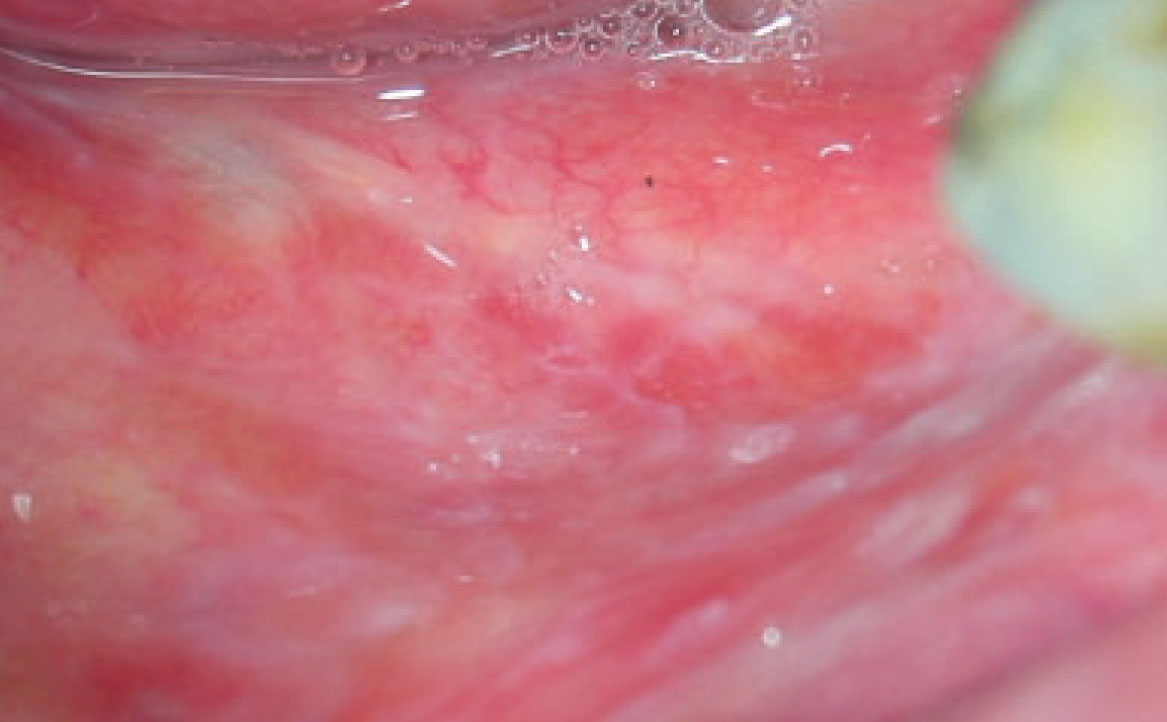
Le lesioni orali caratteristiche del lupus eritematoso mostrano una somiglianza clinica con le manifestazioni del lichen planus orale, presentando zone irregolari di atrofia/erosioni o ulcerazioni, circondate da lesioni reticolari ipercheratosiche. Queste lesioni sono solitamente localizzate principalmente nel palato, nella mucosa geniena, nella mucosa alveolare o gengivale (fig. 4). Dato che il coinvolgimento del palato è poco comune nel lichen planus, la sua presenza potrebbe agevolare la diagnosi differenziale. Nel caso del LE indotto da farmaci, si osserva un miglioramento delle lesioni entro alcuni giorni o settimane dalla sospensione del farmaco causante. Tra i farmaci più frequentemente coinvolti si annoverano l’idralazina e la procainamide (20%) (20). Altri farmaci potenzialmente correlati al LE includono i β-bloccanti, le sulfonamidi, l’isoniazide, la clorpromazina, la metildopa, la penicillamina, la chinidina e gli agenti biologici come gli inibitori anti-TNF (21).
REAZIONI VESCICOLO-BOLLOSE (PEMFIGO VOLGARE E PEMFIGOIDE DELLE MEMBRANE MUCOSE)
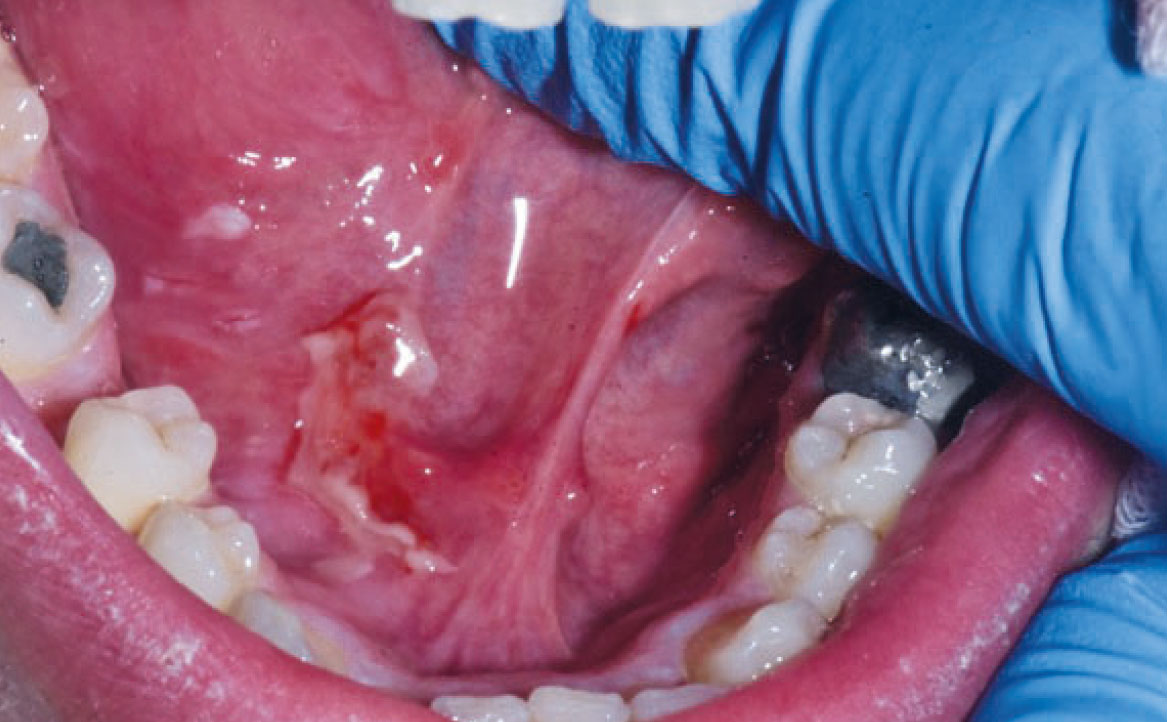
Le patologie vescicole-bollose rappresentano un gruppo di condizioni caratterizzate dalla formazione di vescicole e bolle sulla mucosa orale e sulla cute. Tra queste, il pemfigo volgare è una patologia cronica di natura autoimmune che coinvolge frequentemente la mucosa orale. Le lesioni bollose del pemfigo volgare hanno la tendenza a rompersi facilmente, causando ulcere dolorose. Alcuni farmaci possono indurre lesioni orali clinicamente e istologicamente simili al pemfigo, producendo autoanticorpi diretti contro le molecole desmosomiali e causando acantolisi cheratinocitaria (21). Tra i farmaci più associati a questa condizione vi sono la penicillamina, la rifampicina, il diclofenac e alcuni ACE-inibitori. Inoltre, anche i FANS come il diclofenac, l’ibuprofene e il piroxicam, il fenobarbital, la fenilbutazone, il propranololo e l’eroina possono provocare lesioni simili al pemfigo (fig. 5) (22).
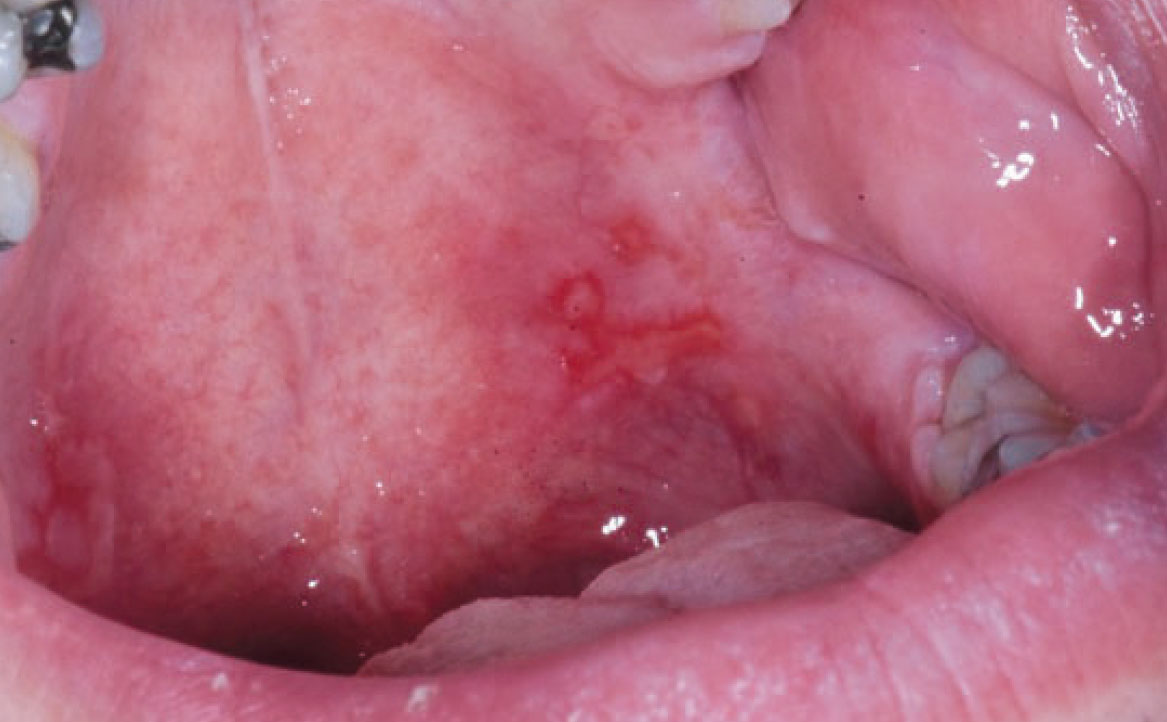
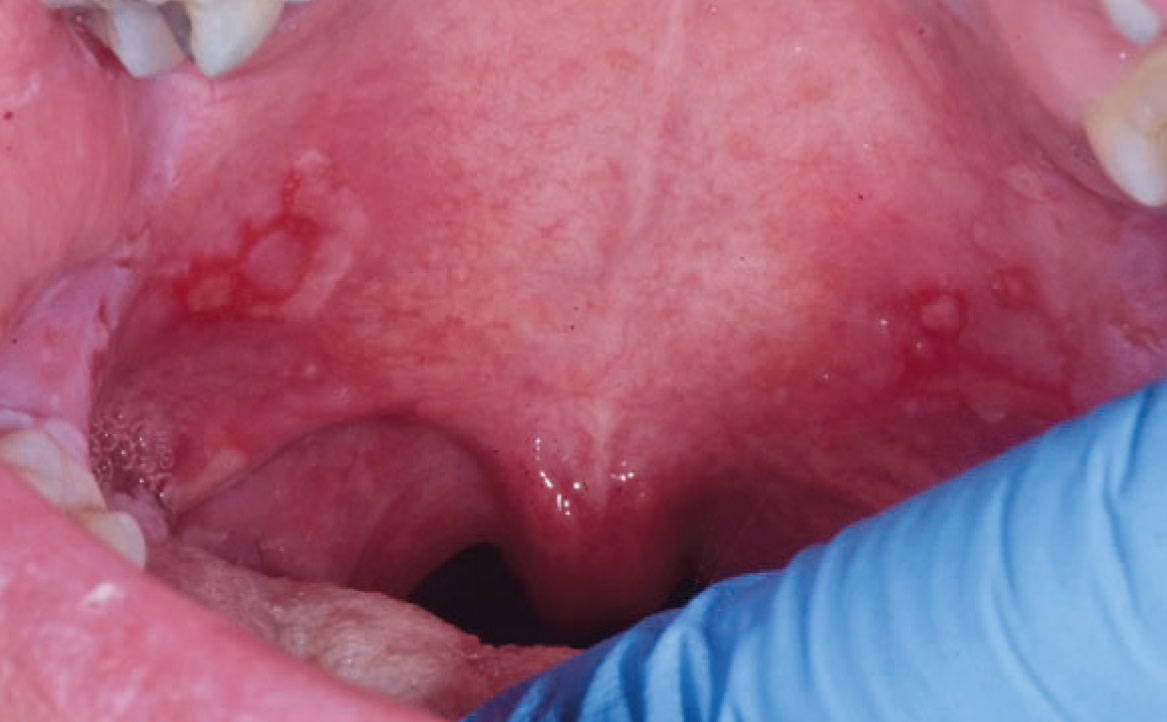
Il pemfigoide delle membrane mucose è un’altra malattia vescicolo-bollosa cronica, caratterizzata dal deposito di IgG, IgA o C3 lungo la membrana basale dell’epitelio. Sebbene simile al pemfigo nel meccanismo patogenetico, il pemfigoide coinvolge gli emi-desmosomi, causando la formazione di bolle sotto-epiteliali. Questa condizione si manifesta con lesioni bollose che interessano principalmente la mucosa orale, la congiuntiva oculare, la mucosa nasale, l’area anogenitale, faringe, laringe ed esofago. Il pemfigoide farmaco-indotto colpisce solitamente individui più giovani rispetto al pemfigoide idiopatico (22). I farmaci comunemente associati a questa forma di pemfigoide includono quelli contenenti componenti tiolici e sulfamidici, oltre ad antiaritmici, antipertensivi, antidiabetici, diuretici, antibiotici, agenti antireumatici, anti-TNF α, antipsicotici e FANS (fig. 6) (23).
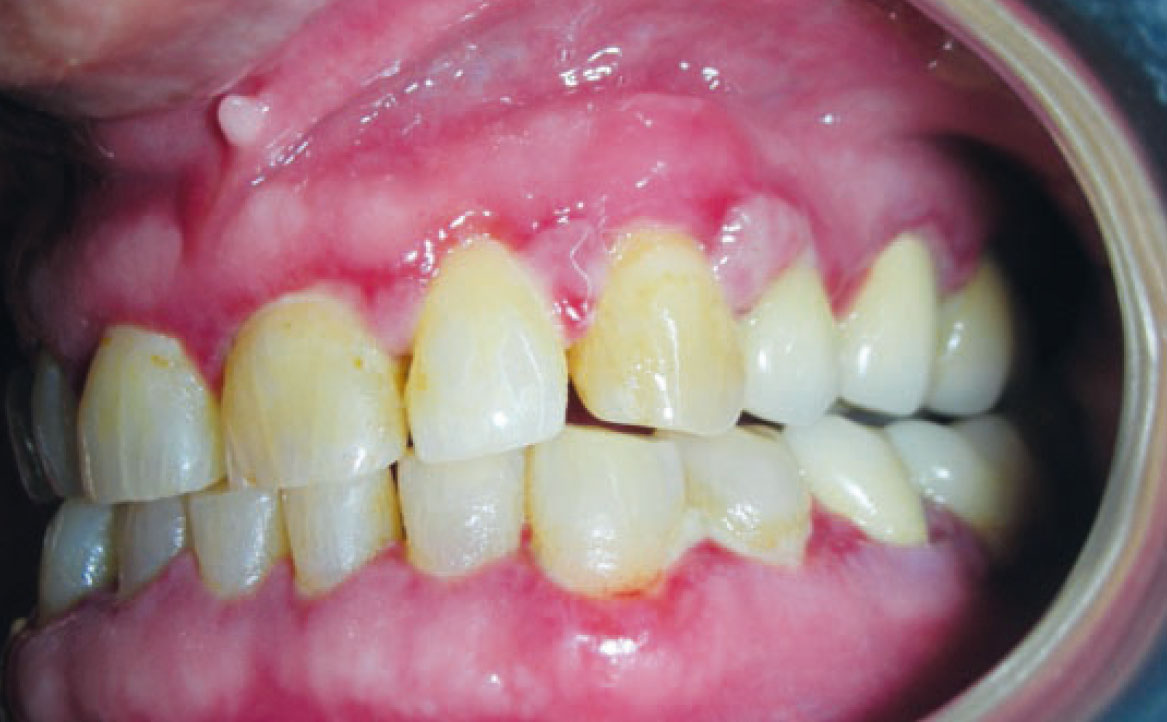
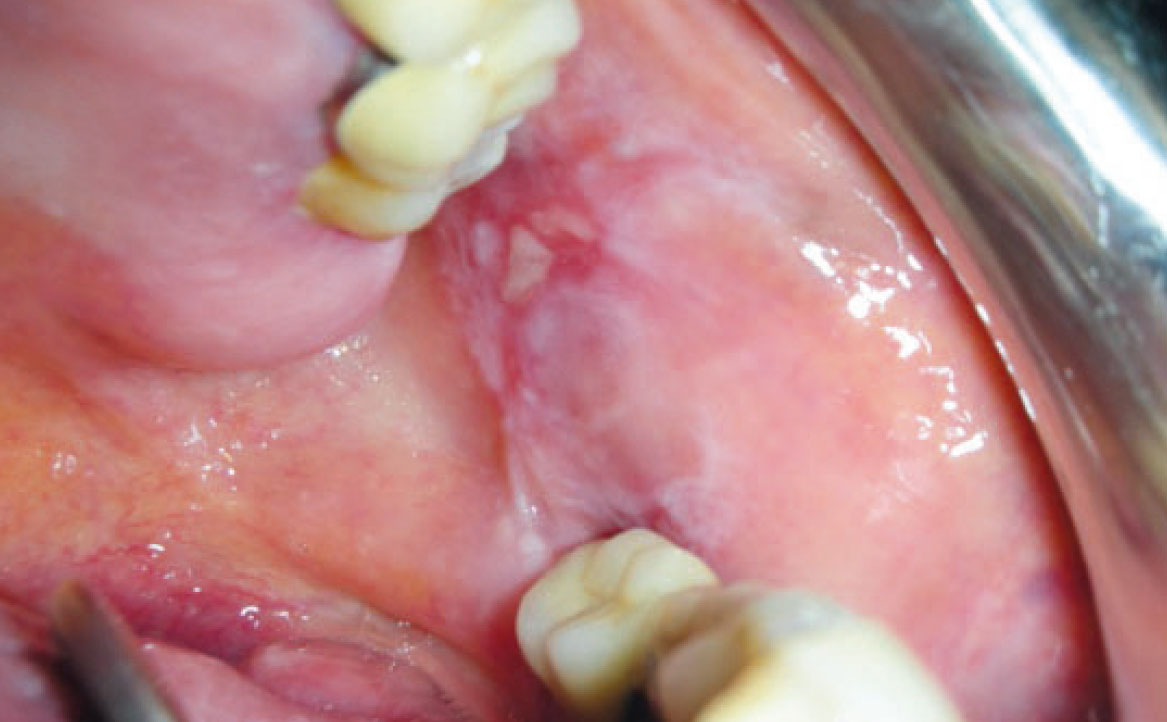
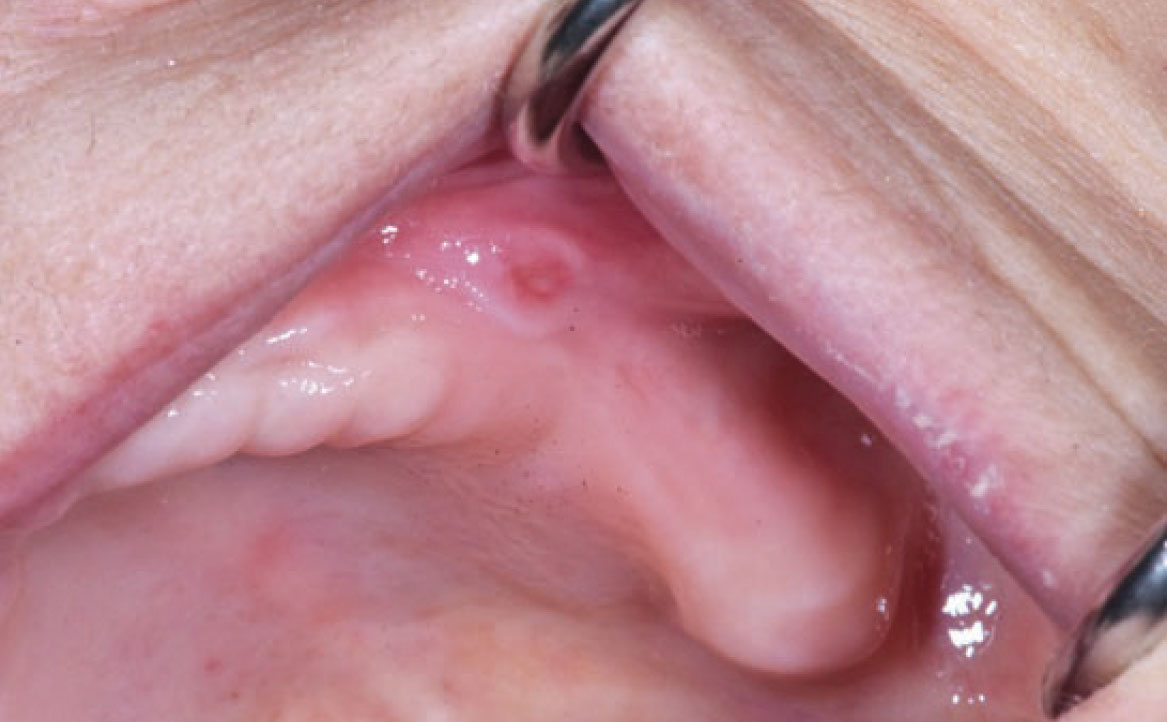
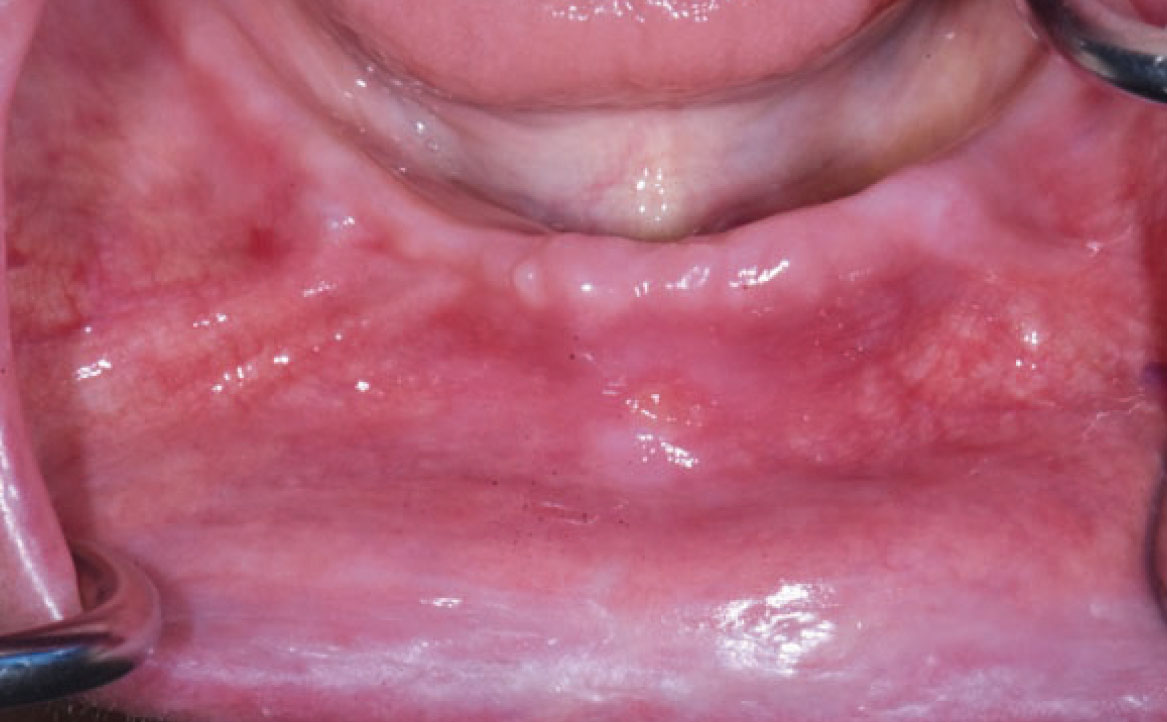
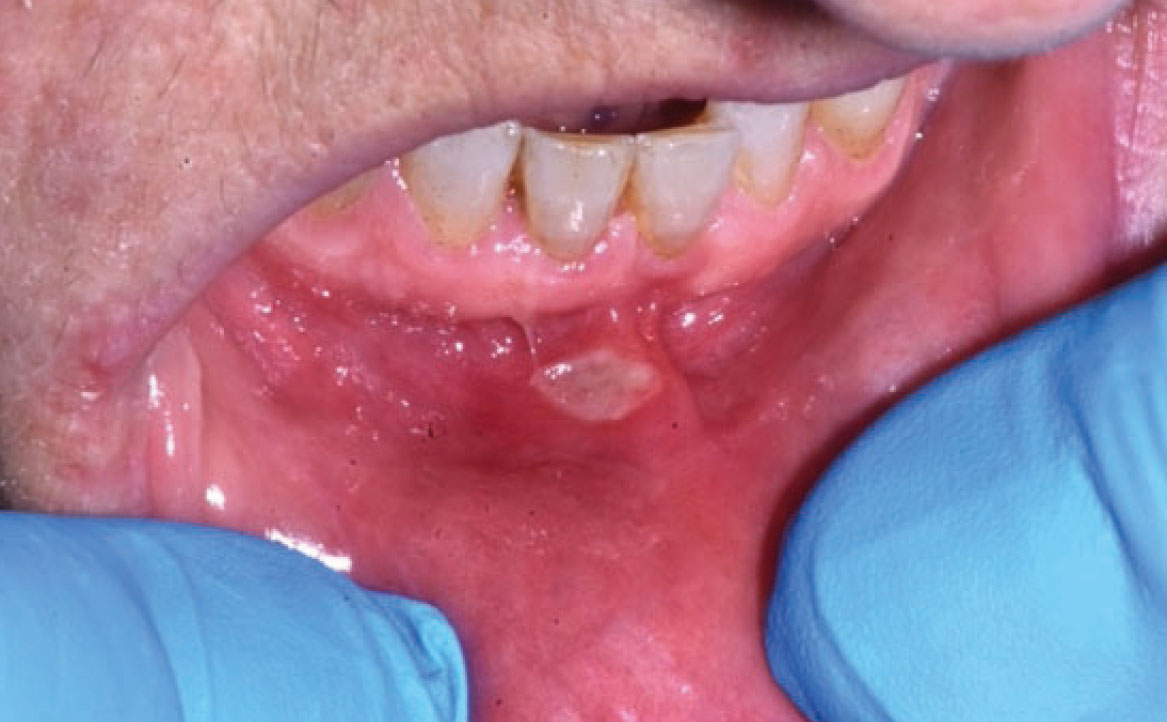
ULCERE SIMIL AFTOSE
Le lesioni ulcerative indotte da farmaci rappresentano un’entità distinta dalle ulcere tipiche della stomatite aftosa ricorrente. Mentre le afte solitamente compaiono nel secondo decennio di vita come ulcere orali ricorrenti, le ulcere da farmaci colpiscono spesso pazienti più anziani e non mostrano necessariamente un pattern periodico; la loro patogenesi non è ancora completamente compresa. Queste lesioni sono spesso singole, isolate, circondate da un alone eritematoso e frequentemente si trovano sul margine laterale della lingua. Le ulcere possono derivare dalla necrosi epiteliale causata dall’applicazione diretta di farmaci sulla mucosa, come l’acido acetilsalicilico, il perossido di idrogeno, le compresse di potassio e i composti contenenti fenolo. Inoltre, diversi farmaci per uso sistemico sono comunemente associati alla comparsa di ulcere orali, tra cui beta-bloccanti (come il labetalolo), broncodilatatori anticolinergici (tiotropio), antiaggreganti piastrinici (clopidogrel), vasodilatatori (nicorandil), inibitori della proteasi, antibiotici (trimetoprim e sulfametoxazolo), farmaci antinfiammatori non steroidei (piroxicam, il rofecoxib e il naprossene), antiretrovirali, farmaci antireumatici antipertensivi e immunosoppressori (fig. 7) (24). Nella sezione dedicata, verranno analizzati i farmaci utilizzati nelle terapie oncologiche correlati a lesioni ulcerative del cavo orale.
PIGMENTAZIONI DELLA MUCOSA ORALE
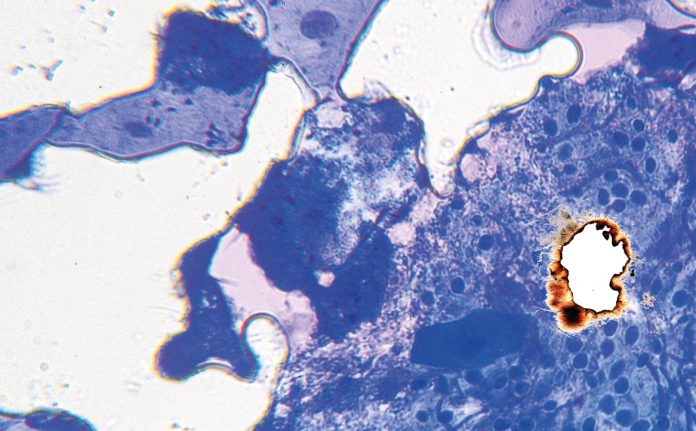
Le pigmentazioni della mucosa orale indotte da farmaci sono alterazioni della colorazione della mucosa che possono verificarsi a seguito dell’assunzione di determinati farmaci. Queste pigmentazioni possono manifestarsi in varie tonalità, compresi il blu, il nero, il marrone e il grigio, e possono interessare diverse aree della mucosa orale, in modo localizzato o diffuso, ma le lesioni sono sempre omogenee e senza aumento di spessore.
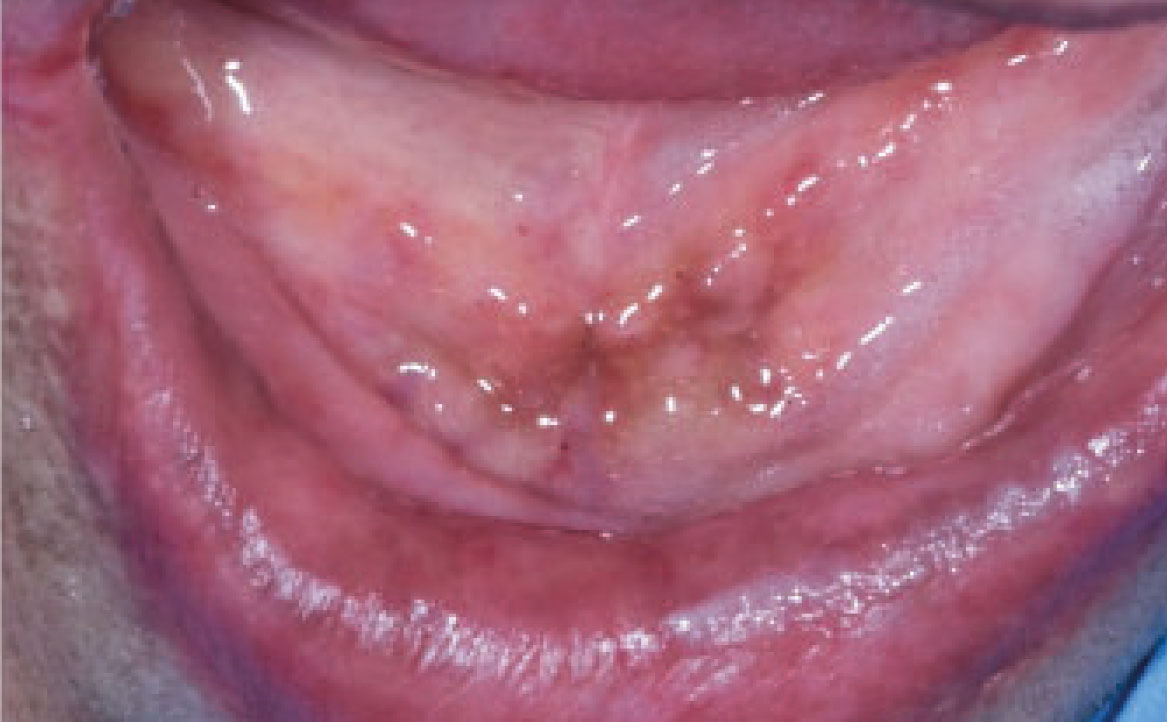
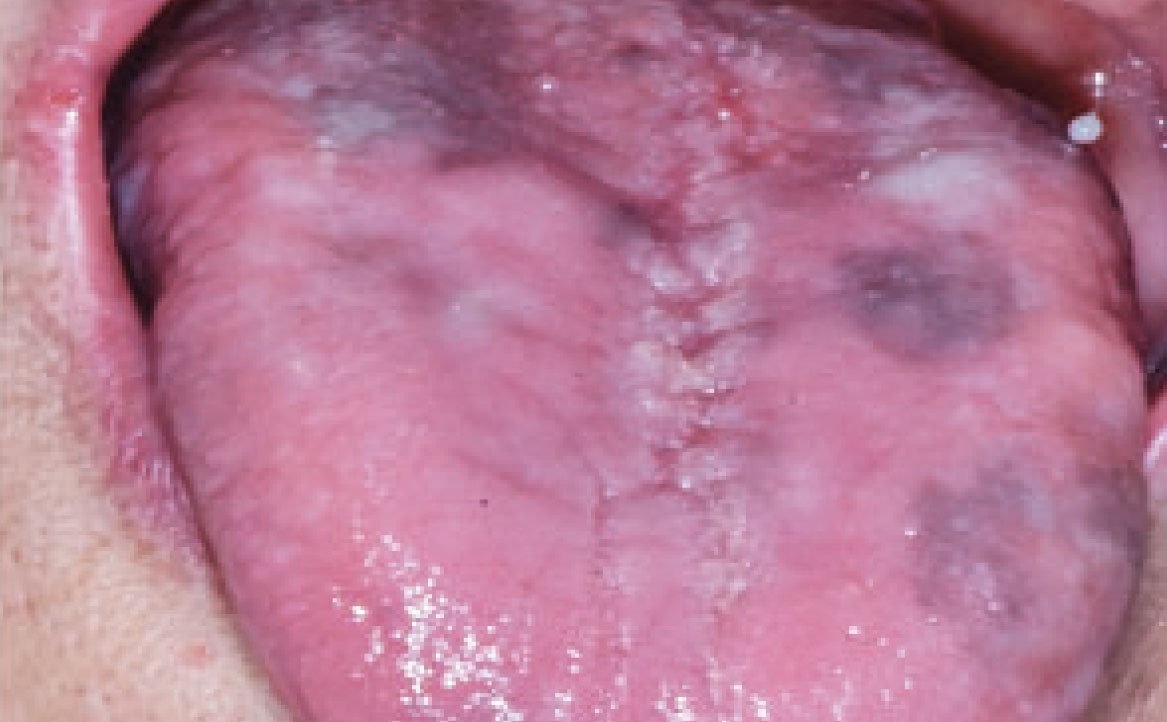
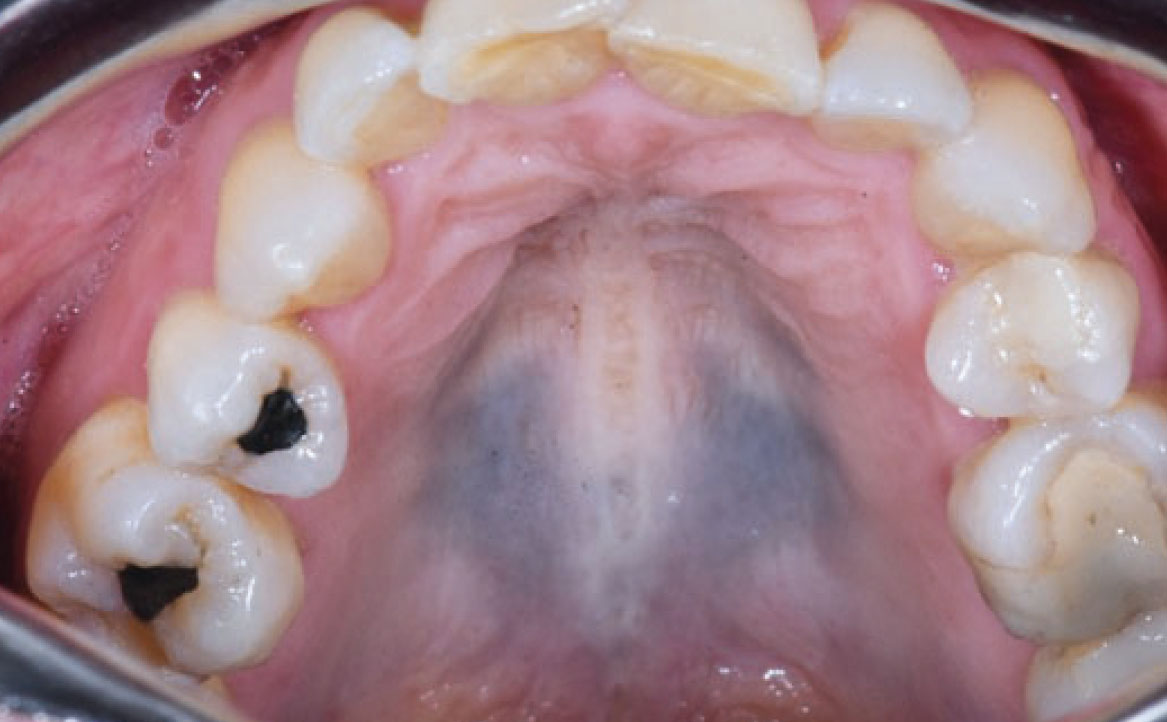
Le pigmentazioni orali causate dai farmaci possono essere classificate in due categorie principali: endogene ed esogene. Le pigmentazioni endogene sono causate dalla deposizione di pigmenti endogeni, come l’emoglobinuria o l’emocromatosi, mentre le pigmentazioni esogene sono il risultato della deposizione di pigmenti esogeni contenuti nei farmaci o nei loro metaboliti (21). Diversi farmaci sono stati associati alla comparsa di pigmentazioni della mucosa orale. Tra questi vi sono alcuni antibiotici come la tetraciclina e la minociclina, che possono causare una pigmentazione bluastra o grigiastra della mucosa. Altri esempi includono farmaci antimalarici come la clorochina e l’idrossiclorochina, che possono causare una pigmentazione marrone o grigiastra, e farmaci antiretrovirali come la zidovudina, che può causare una pigmentazione nera della mucosa (fig. 8) Alcuni farmaci possono indurre la melanogenesi, come contraccettivi orali, clorpromazina, farmaci citotossici come ciclofosfamide e busulfan (25). Pigmentazioni della mucosa orale possono essere indotte da molti altri farmaci, tra cui anche chemioterapici (imatinib, bleomicina, clofazimina, doxorubicina, busulfan, ciclofosfamide). Imatinib, in particolare, utilizzato nel trattamento di alcuni tipi di cancro, tra cui la leucemia mieloide cronica (LMC), è un inibitore della tirosin-chinasi che inibisce la tirosin-chinasi BCR-ABL mutata della LMC. Inoltre, l’imatinib blocca il legame dei ligandi ai recettori c-kit sui melanociti, riducendo l’attività dei melanociti e portando a ipopigmentazione cutanea, ma nella recente letteratura è stato notato che i pazienti in terapia con imatinib sviluppano iperpigmentazione diffusa nel palato duro (26). La diagnosi di pigmentazione correlata all’imatinib dipende da una storia clinica accurata e dalle caratteristiche cliniche specifiche. Le lesioni iperpigmentate sono benigne e non richiedono trattamento (fig. 9).
IPERPLASIA GENGIVALE FARMACO-INDOTTA
Il termine “aumento di volume gengivale farmaco-indotto” si riferisce comunemente a un effetto collaterale di alcuni farmaci utilizzati al di fuori della pratica odontoiatrica, per cui il tessuto gengivale non è il bersaglio previsto. Questi farmaci includono anticonvulsivanti come la fenitoina, che è la molecola più comunemente associata, immunosoppressori come la ciclosporina e calcio-antagonisti come la nifedipina (27) (fig. 10). Questa reazione avversa è principalmente legata a una predisposizione genetica e alla presenza di placca accompagnata da infiammazione gengivale, anche se i meccanismi esatti non sono ancora completamente compresi. La maggior parte dei farmaci responsabili agisce come inibitore dell’afflusso di ioni calcio. Questo porta a una diminuzione dell’assorbimento dell’acido folico nei fibroblasti del tessuto gengivale, il quale è essenziale per il corretto funzionamento della matrice delle metallo-proteinasi e l’attivazione delle collagenasi. Senza questa normale degradazione del collagene, si verifica un accumulo nel tessuto connettivale (28). Il trattamento può essere conservativo o chirurgico, mirando a ottenere un risultato estetico soddisfacente e a ridurre al minimo il disagio e il dolore. Se possibile, la sostituzione del farmaco implicato può portare alla regressione dell’iperplasia, supportata da un adeguato controllo della placca. Altrimenti, la soluzione chirurgica può essere l’unica opzione.
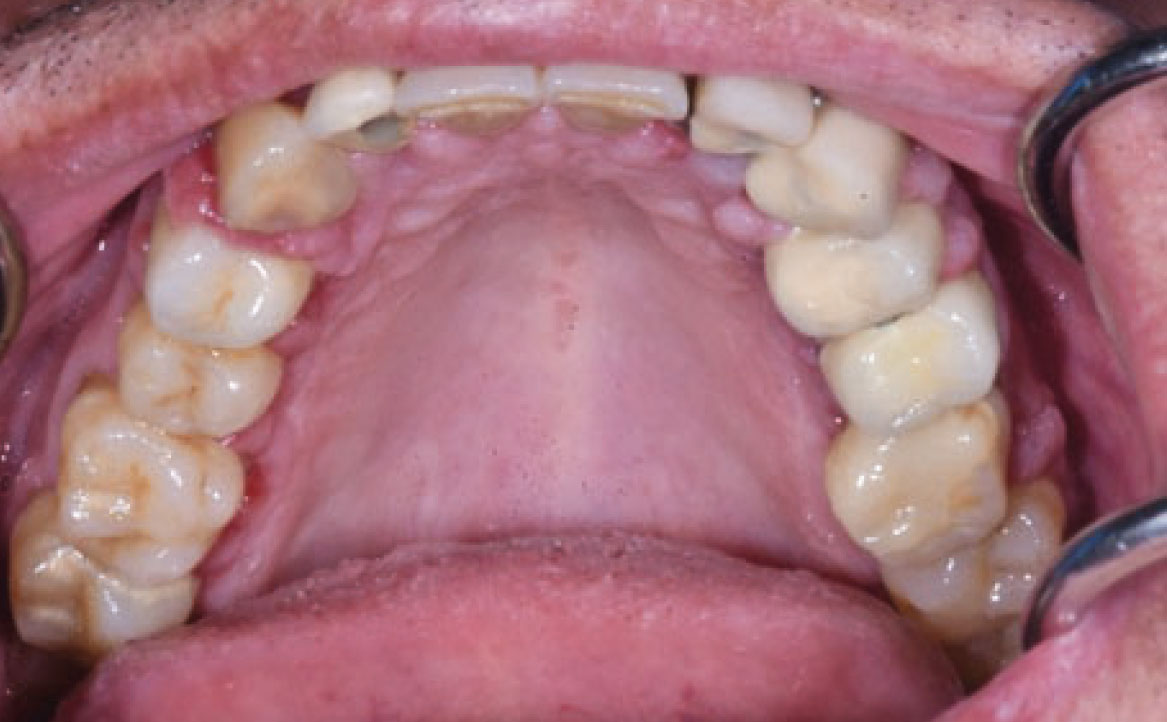
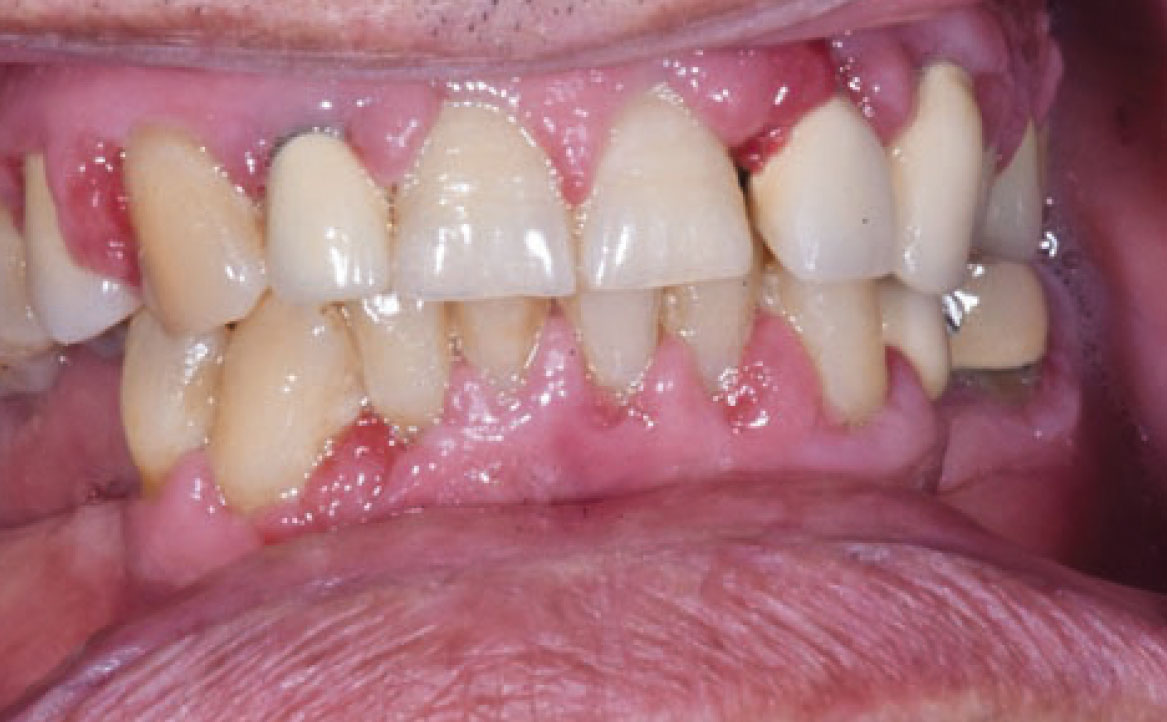
Clinicamente, i pazienti presentano un aumento di volume gengivale con pseudotasche, abbondante accumulo placca e difficoltà durante le manovre d’igiene orale domiciliare. Tale condizione è aggravata dall’infiammazione gengivale, conseguente all’accumulo di placca e tartaro, pertanto, è essenziale educare correttamente i pazienti sui potenziali effetti collaterali prima di iniziare qualsiasi trattamento farmacologico, sottolineando l’importanza di una igiene orale appropriata.
ADR-O DA VACCINAZIONE ANTI-SARS-COV-2
La comprensione delle ADR causate dai vaccini anti-SARS-CoV-2 è fondamentale nel contesto della loro diffusa utilizzazione nella campagna di vaccinazione globale. Mentre la letteratura scientifica ha ampiamente documentato varie forme di ADR associate a questi vaccini, vi è ancora una scarsa comprensione delle reazioni avverse che coinvolgono il cavo orale, aspetto fondamentale, considerando che le ADR-O potrebbero contribuire all’impatto della valutazione complessiva della loro sicurezza.
Una recente revisione sistematica ha analizzato le manifestazioni orali riportate nei pazienti adulti dopo la somministrazione dei vaccini anti-SARS-CoV-2 approvati dall’OMS e pur considerando un campione relativamente limitato di 16 casi, è emerso che le lesioni orali in seguito alla vaccinazione risultano essere un fenomeno raro. Tuttavia, è importante notare che potrebbe esserci una sottostima dei casi a causa della mancanza di documentazione e segnalazione. In particolare, è stata osservata una prevalenza maggiore di lesioni orali nelle donne rispetto agli uomini, con una distribuzione di circa il 68,8% e il 31,2% rispettivamente (29).
Le lesioni orali più comuni sono state le erosioni e le ulcere, con una percentuale del 34,5%. Altre manifestazioni includevano: croste emorragiche, placche e papule bianche, edema, macchie, desquamazione, e vescicole e bolle, riscontrando un legame tra le lesioni orali e i vaccini a mRNA come il BNT162b2 Comirnaty® (Pfizer-BioNTech) e il mRNA-1273 Spikevax® (Moderna). In particolare, nove casi di ADR-O sono diagnosticati dopo il vaccino Pfizer-BioNTech, due dopo il vaccino Moderna, e uno rispettivamente dopo i vaccini AstraZeneca, Serum Institute of India, Sinopharm e Johnson & Johnson; in particolare, otto dopo la prima dose e sette dopo la seconda. In un caso, il tipo di vaccino e la dose non sono stati specificati.
L’insorgenza delle lesioni orali si verifica principalmente dopo la somministrazione del primo e secondo dosaggio, con un intervallo medio di 9,41 giorni. Queste lesioni possono essere considerate come reazioni avverse ritardate, con una correlazione possibile con una risposta immune innescata dalla vaccinazione. Tuttavia, la mancanza di una documentazione completa e omogenea dei casi rappresenta una limitazione importante nella nostra comprensione di questo fenomeno.
Inoltre, è stato osservato che le lesioni orali possono verificarsi in soggetti di età compresa tra i 20 ei 60 anni, con una distribuzione significativa intorno ai 47 anni. Le comorbidità e la storia di COVID-19 dei casi sono risultate essere dati mancanti o poco rappresentati, ostacolando una valutazione approfondita della correlazione tra lo stato di salute del paziente e l’insorgenza delle lesioni orali. In conclusione, le limitazioni dei dati disponibili, rendono necessarie ulteriori ricerche per comprendere appieno la natura di queste lesioni, e considerando lo sviluppo di nuovi vaccini, i risultati presentati potrebbero essere aggiornati e ulteriori studi saranno necessari per evidenziare i fattori che influenzano l’insorgenza di lesioni orali e i fenotipi macro-microscopici specifici in relazione alle caratteristiche dei casi e dei vaccini.
ADR-O IN CORSO DI TERAPIE ONCOLOGICHE
Le conseguenze dei trattamenti oncologici basati su chemio e radioterapia si distinguono in due categorie: gli effetti immediati e quelli a lungo termine. Gli effetti immediati, che si manifestano durante il trattamento e solitamente si risolvono alla sua fine, sono principalmente legati ai danni cellulari e all’infiammazione causati dalla chemioterapia. Al contrario, gli effetti a lungo termine, che si verificano mesi o anni dopo la conclusione del trattamento, sono spesso legati a processi di fibrosi e atrofia tissutale dovuti alla radioterapia.
La mucosite orale è una delle conseguenze immediate più comuni e problematiche, con un’incidenza che varia a seconda del tipo di trattamento: si stima che tra il 30% e il 40% dei pazienti sottoposti a chemioterapia, tra il 60% e l’85% di coloro che ricevono un trapianto di cellule staminali emopoietiche e fino al 90% dei pazienti con carcinoma testa-collo trattati con chemio-radioterapia combinata sviluppino questa condizione (30,31).
La mucosite orale è causata da una serie di eventi interconnessi che coinvolgono danni cellulari, produzione di specie reattive dell’ossigeno e infiammazione. Questi eventi portano all’ulcerazione della mucosa, che rappresenta il picco clinico della malattia e può causare gravi sintomi come dolore e difficoltà alimentari.
Dal punto di vista clinico, l’esordio della mucosite orale è caratterizzato da un’infiammazione della mucosa, evidenziata da un arrossamento diffuso o localizzato, che evolve progressivamente verso lesioni erosive e, infine, ulcerative. Queste ulcere sono solitamente rivestite da membrane biancastre, composte da tessuti necrotici, fibrina e batteri che colonizzano la superficie (fig. 11).
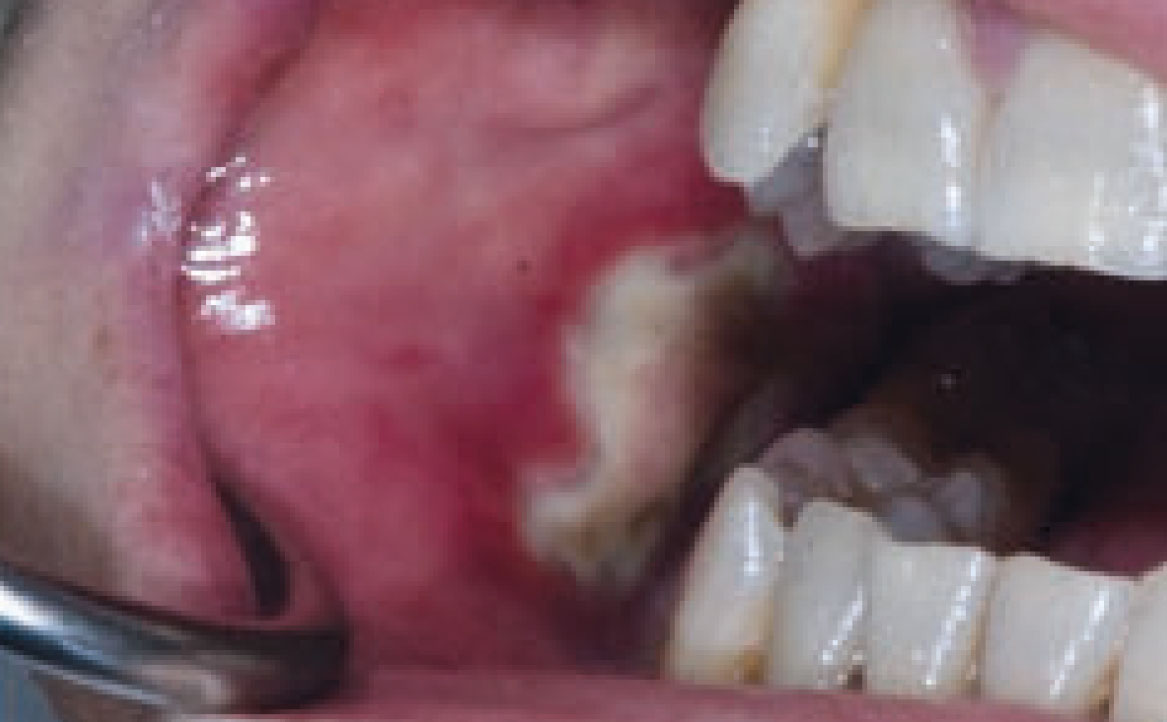
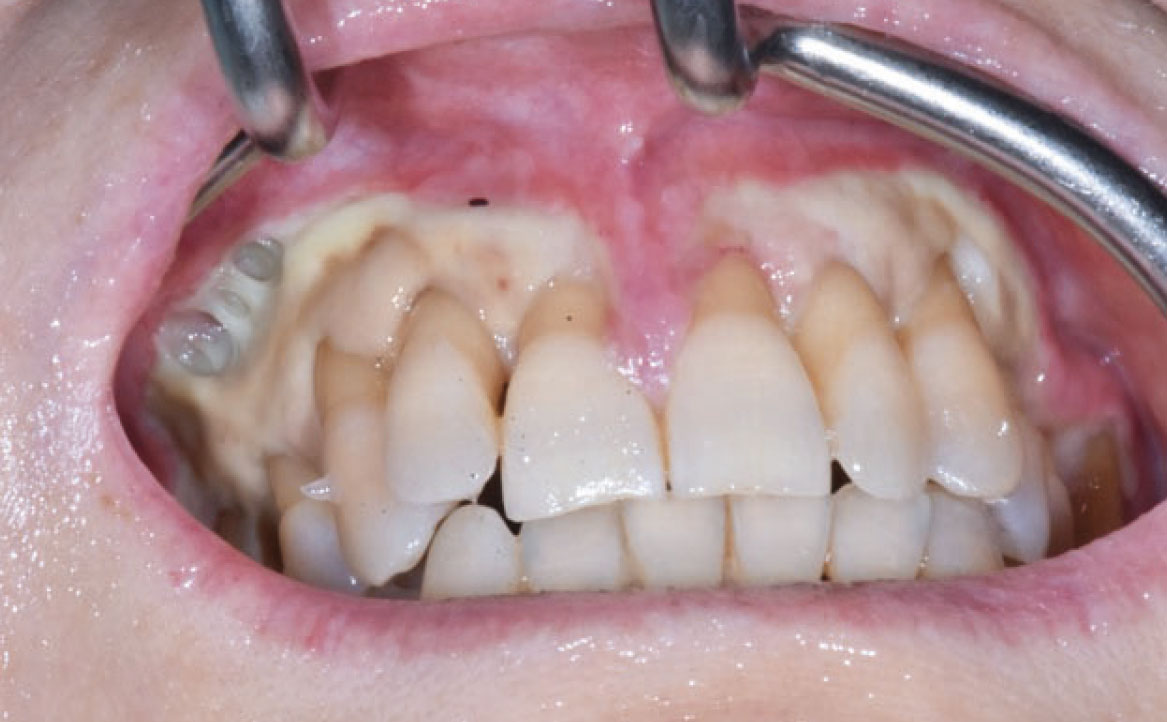
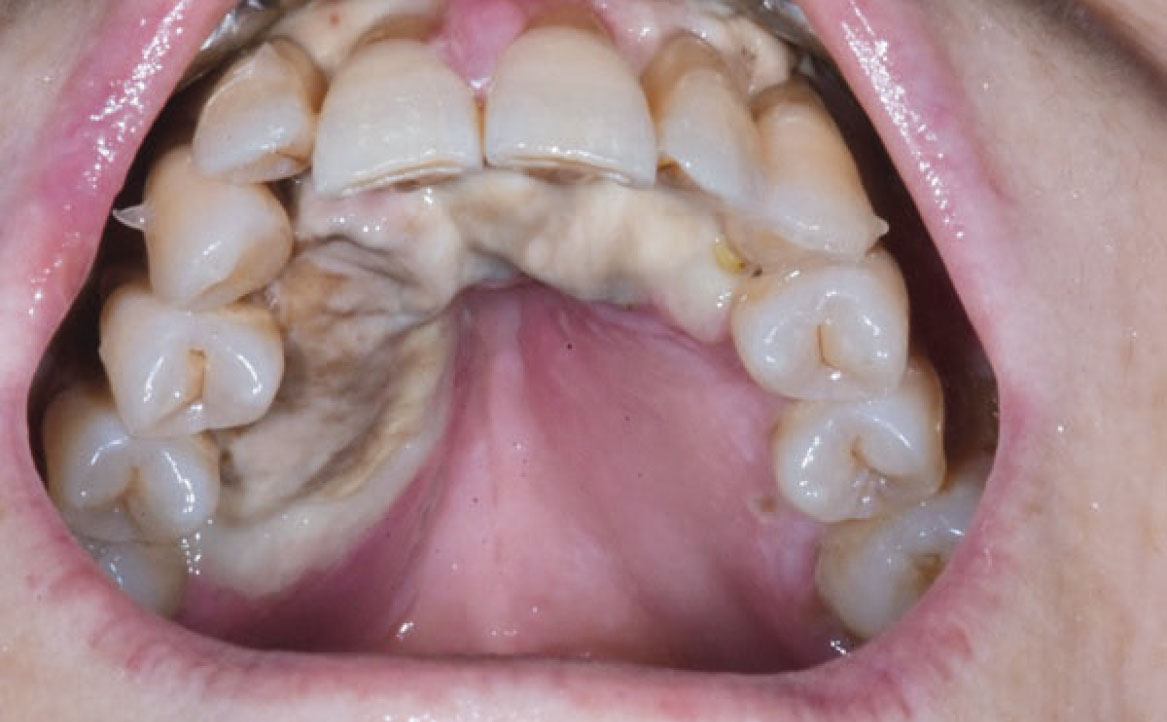
Queste lesioni possono comportare notevoli difficoltà nell’alimentazione, con conseguente rischio di carenze nutrizionali e perdita di peso, talvolta richiedendo l’uso di alternative come il sondino naso-gastrico o la nutrizione parenterale totale, accompagnata spesso dall’uso di analgesici oppioidi (32).
Le implicazioni clinico-funzionali della mucosite orale sono ampie e variegate, includendo difficoltà nella deglutizione, dolore durante la deglutizione, alterazioni del gusto e difficoltà nel parlare, tutte condizioni, queste, che influenzano significativamente la qualità della vita del paziente. Inoltre, il decorso della malattia può essere ulteriormente complicato da infezioni, soprattutto nei pazienti con compromissione del sistema immunitario, con possibilità di riattivazione virale come l’herpes simplex (HSV) o sviluppo di infezioni fungine come la candidosi orale (33).
L’occorrenza e la gravità della mucosite sono strettamente correlate al tipo di chemioterapia utilizzata, alle dosi somministrate e alla durata del trattamento. Farmaci come gli antimetaboliti, i derivati del platino, i taxani, le antracicline, l’irinotecan e gli agenti alchilanti possono aumentare il rischio di sviluppare mucosite orale, con variazioni nella gravità e nella localizzazione delle lesioni tra i diversi farmaci e le loro combinazioni (tab. 2).
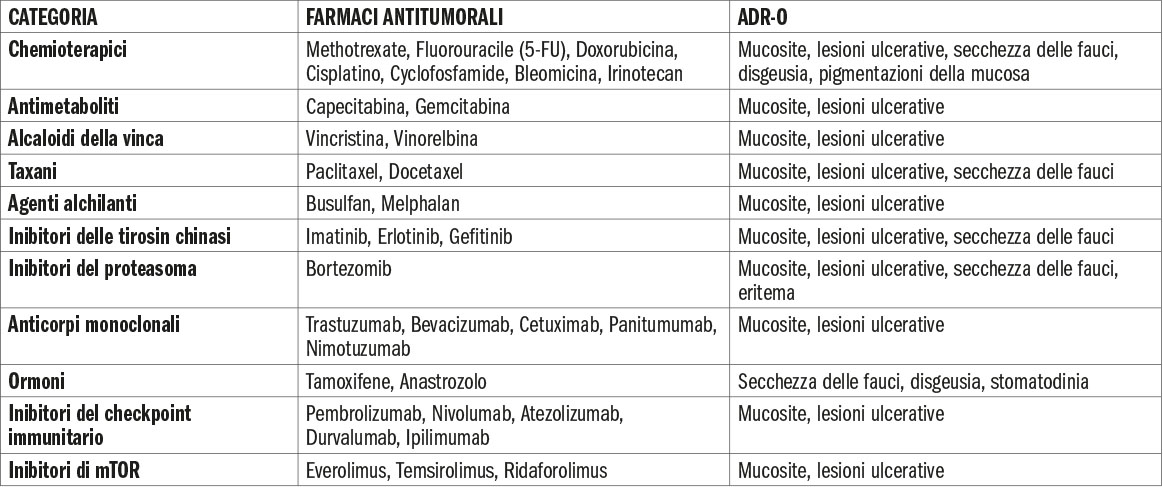
Nel campo dell’oncologia, le terapie mirate o a bersaglio molecolare rappresentano un’importante innovazione che si affianca alla chemio-radioterapia tradizionale. Questi farmaci, conosciuti come agenti “targeted”, comprendono molecole a basso peso molecolare (come gli inibitori di tirosin-chinasi terminanti in -Nib e gli inibitori di mTOR terminanti in -Rolimus) e anticorpi monoclonali (terminanti in -Mab). Il loro obiettivo è inibire selettivamente specifici fattori di crescita, recettori cellulari e vie di trasduzione del segnale all’interno delle cellule tumorali. Questa precisione d’azione si traduce spesso in un’efficacia terapeutica maggiore e in un profilo di tossicità generalmente inferiore rispetto alla chemioterapia convenzionale.
Tuttavia, è importante notare che anche i farmaci a bersaglio molecolare possono causare effetti collaterali, che possono differire da quelli osservati con la chemioterapia tradizionale. Ciò sottolinea l’importanza di un monitoraggio attento e di una gestione specifica degli effetti collaterali in questa categoria di pazienti.
Ad esempio, gli inibitori di mTOR come everolimus, tenserolimus o ridaforolimus sono associati a una maggiore tossicità orale, caratterizzata dalla comparsa di lesioni ulcerative note come mIAS (mTOR inhibitor-associated stomatitis) che si presenta di solito entro 5 giorni dal primo ciclo di trattamento con un’area necrotica centrale circondata da un alone eritematoso. Sebbene possa causare dolore intenso, tende a migliorare o risolversi spontaneamente durante la terapia, di solito senza la necessità di interrompere il trattamento (34,35).
Allo stesso modo, gli inibitori del recettore del fattore di crescita epidermico (EGFR), come Cetuximab, Panitumumab e Nimotuzumab, e gli inibitori delle tirosin-chinasi (TKi) come Erlotinib e Gefitinib, sono associati allo sviluppo di mucosite orale, legata al ruolo cruciale dell’EGFR wild-type nella regolazione delle cellule epidermiche ed epiteliali. Tuttavia, la tossicità orale causata da questi farmaci si manifesta di solito con eritema moderato e lesioni simili ad afte, con un’incidenza inferiore all’1%, e raramente richiede una modifica o interruzione del trattamento (36).
Inoltre, ADR-O caratterizzate da lesioni ulcerative sono state riportata anche come un evento avverso correlato all’immunoterapia (irAE) in pazienti trattati con farmaci che influenzano gli immuno-checkpoint, come gli anti-PD1 (come pembrolizumab e nivolumab), anti-PDL1 (come atezolizumab e durvalumab) o anti-CTLA4 (come Ipilimumab), con un’incidenza stimata intorno all’8% (37,38).
DIAGNOSI DELLE ADR-O
Il riconoscimento precoce delle reazioni avverse ai farmaci (ADR-O) è cruciale per il benessere del paziente e la gestione ottimale dei costi sanitari. Questa pratica implica la tempestiva cessazione del farmaco responsabile, prevenendo così l’evolversi di complicazioni che potrebbero risultare irreversibili. Tale identificazione rapida facilita l’adozione di terapie personalizzate per alleviare il disagio del paziente, riducendo allo stesso tempo la necessità di trattamenti onerosi e non necessari.
Inoltre, il riconoscimento precoce delle ADR-O e la loro segnalazione ad AIFA contribuisce significativamente alla sicurezza dei farmaci, fornendo dati cruciali per una valutazione costante della loro efficacia e sicurezza. Questo processo non solo garantisce un trattamento farmacologico sicuro ed efficace per i pazienti, ma contribuisce anche a ridurre il rischio di future reazioni avverse.
Per una diagnosi accurata delle ADR-O è essenziale considerare una serie di fattori indicativi, come riportato nella tabella 3.

A seguire, una disamina dei criteri essenziali per l’identificazione delle ADR-O, che includono: l’anamnesi del paziente, l’esame obiettivo ed eventuali test specifici.
ANAMNESI DEL PAZIENTE
La raccolta anamnestica è cruciale nel processo diagnostico delle ADR-O, suddividendosi in categorie informative essenziali per una registrazione dettagliata che includono: ▼

L’anamnesi patologica remota offre un contesto prezioso per la diagnosi differenziale, fornendo tracce diagnostiche, identificando quadri patologici cronici, e valutando gli esiti dei trattamenti precedenti.
L’anamnesi allergologica riveste importanza cruciale, raccogliendo con precisione informazioni sulle allergie note del paziente, incluse quelle a sostanze non farmacologiche. Questo processo facilita la diagnosi differenziale delle ADR-O, fondamentale nell’approccio clinico.
Una volta acquisita una completa e dettagliata anamnesi medica, si pone il compito di determinare se la lesione o il disturbo in questione possa essere direttamente attribuita al farmaco assunto dal paziente. Tale compito diviene ancor più complesso nei casi di poli-farmacoterapia, in cui più farmaci sono concomitantemente in uso. La valutazione della causalità richiede un approccio metodologico mirato all’analisi di differenti parametri (40).
Relazione temporale
La relazione temporale tra l’assunzione del farmaco e l’insorgenza della reazione è eterogenea e può variare considerevolmente. La reazione può manifestarsi immediatamente dopo l’assunzione del farmaco (tipo B), oppure emergere dopo un periodo variabile dalla somministrazione (tipo C, D). In alcuni casi, la reazione può presentarsi solo al termine del ciclo terapeutico (tipo E). Questa diversità temporale riveste grande importanza nella diagnosi e nella valutazione della correlazione causale tra il farmaco e l’ADR-O. È quindi essenziale esaminare attentamente ciascun caso, considerando le specifiche sfumature temporali, per giungere a una conclusione accurata sulla causalità.
Corrispondenza con il profilo farmacologico
La valutazione dell’aderenza della presentazione clinica dell’ADR-O al profilo farmacologico ed allergologico dei farmaci sospettati mira a determinare se i sintomi osservati sono in linea con gli effetti noti di un particolare farmaco o compatibili con una reazione allergica. Tuttavia, non tutte le ADR sono state riconosciute per tutti i farmaci sul mercato, specialmente per molecole farmacologiche nuove o con meccanismi d’azione complessi. Questa consapevolezza è fondamentale poiché una discrepanza tra la reazione e il profilo noto del farmaco non dovrebbe automaticamente escludere l’associazione tra il farmaco e la reazione avversa, considerando possibili meccanismi d’azione poco compresi o risposte individuali del paziente.
Esame obiettivo e valutazione odontoiatrica specialistica
L’esame obiettivo del cavo orale è necessario per comprendere appieno la salute del cavo orale e identificare le eventuali manifestazioni delle ADR-O e dei fattori contribuenti ai sintomi. Questa procedura deve comprendere un esame approfondito della testa e del collo, con valutazione visiva e tattile della mucosa orale. Gli obiettivi principali includono l’analisi delle lesioni mucose e lo studio dello stato di salute oro-dentale-parodontale. È importante raccogliere informazioni sulle abitudini di igiene orale del paziente e identificare eventuali trattamenti odontoiatrici pregressi o recenti, poiché tali procedure possono influenzare la manifestazione delle ADR-O. Inoltre, va anche indagato l’uso di prodotti per l’igiene orale, poiché alcuni ingredienti possono causare reazioni avverse, così come la possibilità di sovradosaggio o intossicazioni accidentali.
Indagini diagnostiche specifiche
Salvo per effetti tossici organo-specifici, attualmente mancano strumenti diagnostici specifici per definire con certezza il rischio di ADR-O. Tuttavia, ci sono metodologie diagnostiche specializzate per confermare lesioni orali legate ai farmaci. Escludendo le reazioni di tipo E, la risposta alla sospensione del farmaco, considerato potenzialmente causativo, potrebbe essere importante nel processo diagnostico. Se la sospensione del farmaco è possibile e l’effetto avverso scompare, si può confermare la correlazione causale mediante la re-somministrazione controllata del farmaco.
Se, dopo la re-somministrazione, la reazione avversa si ripresenta in modo simile o identico, è un forte indizio di correlazione causale, ma questa “rechallenge” potrebbe essere pericolosa in alcuni casi. Questo approccio è importante ma delicato nella valutazione delle ADR e dovrebbe essere usato con cautela, rispettando i principi etici e il benessere del paziente, in quanto potrebbe comportare rischio di anafilassi e dovrebbe essere eseguito in un ambiente ospedaliero controllato. Inoltre, se fosse possibile sostituire facilmente il farmaco ritenuto responsabile, la “rechallenge” potrebbe essere considerata non etica (41).
Se diversi farmaci sono stati identificati come possibili cause, è consigliabile sospendere sequenzialmente i farmaci non essenziali, preferibilmente uno alla volta, valutando attentamente la risposta del paziente. Il periodo di osservazione sarà adattato in base all’eliminazione del farmaco dall’organismo e al tipo di reazione: se il paziente mostra miglioramenti, si possono considerare alternative terapeutiche; in caso di assenza di miglioramenti, si sospende il successivo farmaco più probabile, ripetendo il ciclo. Se alcuni farmaci sospesi sono essenziali per il paziente, si può valutare la loro reintroduzione o, se sospettati come causa di ADR-O, sostituirli con farmaci appropriati, prestando attenzione alle reazioni crociate. La reintroduzione dei farmaci essenziali deve essere graduale, iniziando con l’agente meno probabile come causa della reazione.
Diverse altre procedure diagnostiche possono individuare allergie da farmaci. Tuttavia, sono limitate poiché molte reazioni derivano da metaboliti difficili da rilevare. Nelle reazioni di tipo immediato, la valutazione dei livelli di triptasi può risultare utile poiché rappresenta un indicatore della degranulazione dei mastociti. Per rilevare le reazioni di tipo immediato IgE, si possono eseguire test cutanei. L’esecuzione del patch test si dimostra cruciale nella valutazione della possibilità di reazioni ritardate applicando allergeni specifici sulla pelle del paziente per un periodo di 48-72 ore, identificando quelli responsabili (42).
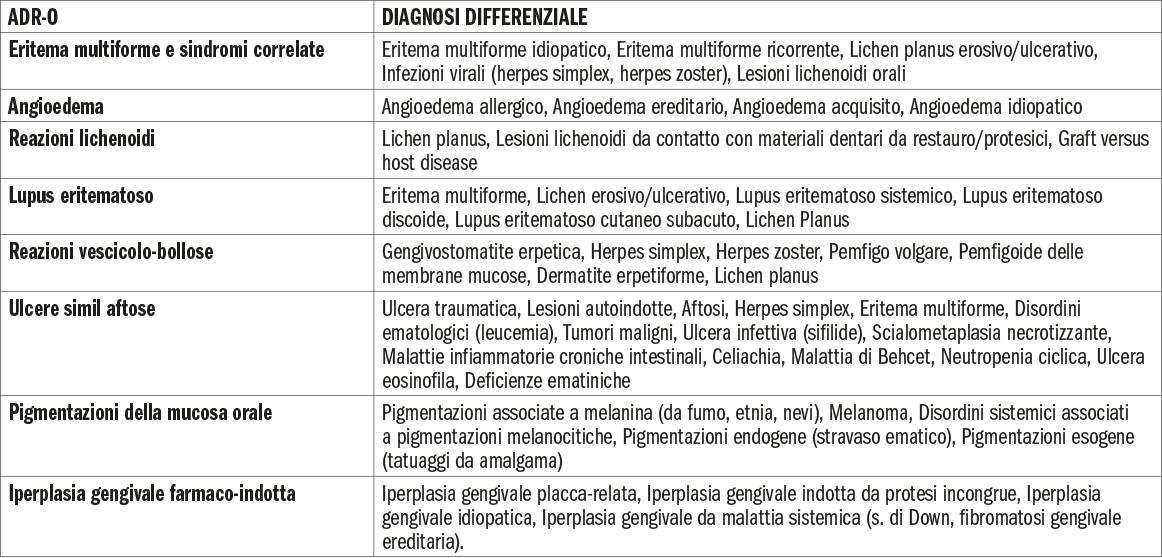
In conclusione, risulta essenziale effettuare una diagnosi differenziale accurata, poiché queste lesioni possono manifestarsi in modi simili ad altre condizioni orali comuni, come ulcere traumatiche, stomatiti aftose ricorrenti, infezioni microbiche, patologie oncologiche, malattie autoimmuni e altri disordini (tab. 4). Una corretta identificazione della causa sottostante è fondamentale per determinare il trattamento più appropriato e per prevenire complicazioni. Quindi, la gestione delle lesioni orali indotte da farmaci richiede un’approfondita valutazione della storia clinica del paziente, compresa l’anamnesi farmacologica, insieme a un esame clinico dettagliato della bocca e dei tessuti circostanti. Questo approccio multidisciplinare, completatato dalla segnalanazione all’ente regolatore (AIFA per l’Italia) della ADR-O, consente una gestione completa e mirata delle ADR-O, ottimizzando così i risultati clinici e migliorando la qualità della vita del paziente.
Ai fini di implementare su tutto il territorio italiano la conoscenza delle ADR in odontoiatria, è stato sviluppato il progetto “ADR in Odontoiatria nell’era informatica: dalla segnalazione alla visita specialistica con un click” (supportato con fondi AIFA multiregionali). Questo articolo si inserisce nel contesto del progetto AIFA, sottolineando l’importanza e l’innovazione della nostra iniziativa nel migliorare la gestione delle reazioni avverse ai farmaci in odontoiatria su scala nazionale. Questo progetto, che al meglio della nostra conoscenza non ha simili in Europa, è stato sviluppato per avviare il miglioramento della conoscenza delle ADR-O, il loro riconoscimento clinico, la segnalazione ad AIFA e la gestione clinica delle stesse, prevedendo la creazione e la divulgazione dei prodotti che seguono.
1. Questionario sulla conoscenza e segnalazione delle reazioni avverse a farmaci in odontoiatria
Questo strumento mira non solo a valutare le loro conoscenze e attitudini verso la segnalazione, ma anche a sensibilizzarli sul dovere di segnalare tali eventi. Il questionario rappresenta il primo obiettivo realizzato, consentendo di indagare la consapevolezza e le conoscenze nell’ambito delle ADR-O dei professionisti della salute mediante domande mirate e pertinenti, al fine di ottenere un risultato che rispecchi la realtà.
2. Atlante delle comuni reazioni avverse a farmaci in odontoiatria
L’atlante svolge un ruolo guida, ma si configura anche come una risorsa formativa per medici, odontoiatri, igienisti e studenti. Offrendo non solo indicazioni pratiche, ma arricchendo l’esperienza professionale con elementi educativi, l’atlante contribuisce così alla crescita continua delle competenze in ambito medico e odontoiatrico. Attraverso la selezione di ciascuna sezione relativa alle reazioni avverse, gli utenti hanno la possibilità di esplorare una breve ma completa descrizione di ogni specifica reazione. Ogni descrizione è accompagnata da immagini esplicative e l’indicazione delle classi di farmaci associati alla manifestazione della suddetta reazione. Ogni categoria di farmaci nell’elenco è progettata per essere interattiva, offrendo agli utenti la possibilità di esplorare un elenco dettagliato di tutte le reazioni avverse ai farmaci correlate a quella specifica classe. In questo modo, l’utente può ottenere una comprensione approfondita delle possibili manifestazioni avverse legate a una particolare categoria di farmaci con un semplice clic.
3. Sinossi dei principali farmaci associati alle reazioni avverse a farmaci in odontoiatria
Nella sezione della “Sinossi”, gli utenti hanno accesso a un elenco esauriente delle principali classi di farmaci, congiuntamente alle reazioni avverse a farmaci della cavità orale (ADR-O) più rilevanti associate a ciascuna classe. Questa funzionalità offre una panoramica dettagliata e organizzata, facilitando la comprensione delle connessioni tra le diverse classi di farmaci e le rispettive ADR-O. Ogni classe di farmaco in elenco è a sua volta cliccabile e permette di accedere a tutte le reazioni avverse a farmaci che possono essere causate dalla stessa.
4. Test di autovalutazione su ADR anonimo e gratuito (fig. 15)
Il test di autovalutazione consente agli utenti di accedere alla piattaforma di self-e-learning. Questa piattaforma è stata realizzata per consentire l’auto-valutazione da parte degli utenti in merito alla conoscenza e comprensione delle ADR-O. Il self-e-learning costituisce un’evoluzione in materia di apprendimento; infatti, la piattaforma è fruibile in qualsiasi momento e da qualsiasi luogo, consentendo agli studenti e ai professionisti di personalizzare il loro percorso e di accedere in modo veloce, flessibile e autonomo. Tale approccio aiuta gli utenti a sviluppare gradualmente le proprie competenze e la comprensione delle ADR-O. Ogni questionario a scelta multipla può essere utilizzato per valutare la conoscenza e la comprensione dei disturbi orali potenzialmente e richiede circa 20 minuti per essere completato. Per completare con successo la valutazione, è necessario ottenere un punteggio superiore all’60% (6/10). Dopo aver completato il questionario, l’utente riceverà un feed-back dettagliato sulle risposte corrette fornite. Per ciascun quesito, avrà la possibilità di consultare la percentuale di risposte date dagli altri utenti e accedere a un approfondimento specifico relativo a quella domanda. Questo processo non solo fornisce un resoconto personalizzato delle prestazioni, ma offre anche un confronto con le risposte degli altri partecipanti, facilitando così una comprensione più approfondita degli argomenti trattati nel questionario. I tre test presentano una progressione graduale nella difficoltà delle domande, questo permetterà di sperimentare un apprendimento efficace e costruttivo, affinando le abilità e le conoscenze passo dopo passo. Attraverso questa esperienza di autovalutazione, sarà possibile, per ciascun utente, saggiare la preparazione riguardo le ADR-O, accrescendo la sicurezza professionale. Inoltre, si avrà l’opportunità di restare sempre aggiornato sulle ultime scoperte nel mondo delle ADR-O.
5. Formazione continua a distanza (FAD) relativa alle reazioni avverse a farmaci in odontoiatria
La Formazione a Distanza (FAD), proposta a tutti i medici, sia specialistici sia non, rap- presenta un elemento essenziale nei risultati tangibili del progetto su ADR-O. Questa modalità continua di apprendimento offre agli operatori sanitari, indipendentemente dalla loro specializzazione (medici, odontoiatri e igienisti dentali), gli strumenti e le risorse necessari per ampliare le loro competenze e conoscenze nel campo specifico del- la segnalazione di reazioni avverse a farmaci nella cavità orale (ADR-O). La flessibilità e la costante accessibilità della FAD sono pensate per garantire un percorso formati- vo personalizzato, adattabile alle diverse esigenze professionali di medici specializzati e non specializzati. Il corso FAD “ADR in odontoiatria nell’era informatica: dalla segnalazione alla visita specialistica con un click” è gratuito e prevede il rilascio di dieci (10) crediti ECM.
6. MedOral, piattaforma digitale e applicazione smartphone-based per teleconsulto e segnalazione delle reazioni avverse a farmaci in odontoiatria (ADR-O), fruibile, mediante applicazione per smartphone, da medici, odontoiatri e igienisti dentali
All’interno del progetto è stata sviluppata “Med-Oral” (derivante da una implementazione della piattaforma Aziendale Olo-Health), un’avanzata piattaforma digitale concepita per il teleconsulto e la segnalazione delle reazioni avverse a farmaci in odontoiatria (ADR-O). Questo strumento innovativo è accessibile tramite un’applicazione per smartphone, pensata per coinvolgere medici, odontoiatri e igienisti dentali. La piattaforma ospita un sistema di tele-consulenza online gestito da esperti in medicina orale. Attraverso l’utilizzo gratuito dell’app, medici, odontoiatri e igienisti dentali possono richiedere supporto per l’identificazione e la segnalazione ad AIFA delle reazioni avverse a farmaci in odontoiatria. Questa iniziativa non solo intensifica l’efficacia della farmacovigilanza, ma stimola anche l’innovazione nella gestione delle ADR-O. Facilitando la connessione tra i professionisti della salute in zone geografiche remote e i medici specialisti del territorio, si realizza un ponte virtuale senza impatto rilevante sul bilancio sia pubblico che privato dei pazienti. In conclusione, l’odontoiatria, in costante evoluzione con l’introduzione di nuovi farmaci e la scoperta di nuove ADR-O, attraverso questo progetto scientifico ed editoriale può attingere a una risorsa dinamica per studenti e professionisti della salute. Questo contribuisce a stimolare una cultura di apprendimento continuo all’interno della comunità odontoiatrica, mirando a garantire una pratica basata sull’evidenza.
Ringraziamenti: Questa ricerca è stata supportato dal progetto “ADR in Odontoiatria nell’era informatica: dalla segnalazione alla visita specialistica con un click” (finanziato da fondo per progetti di farmacovigilanza attiva AIFA).